-
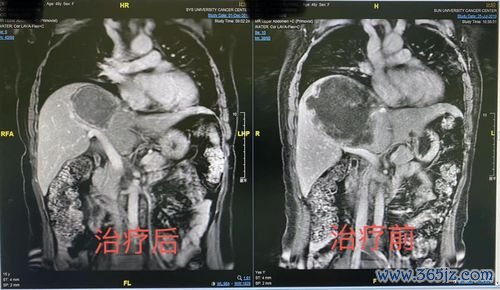
脑转移癌-肺癌脑转移头痛呕吐,放疗科医生说全脑放疗后能缓解
肺癌是常见的恶性肿瘤,其病程中发生脑转移的概率高达20%-65%,这已成为影响患者生存质量与预后的关键因素。脑转移瘤一旦形成,常因占位效应和颅内压升高引发一系列神经系统症状,其中以持续性头痛、恶心呕吐最为常见且令患者痛苦不堪。在自然病程下,若不进行干预,患者的生存期往往非常有限。随着肿瘤治疗手段的不断进步,放射治疗,尤其是全脑放疗,已成为控制脑转移、缓解神经...
2026-04-14
-
胃淋巴瘤-胃部不适CT发现胃壁增厚,胃镜活检淋巴瘤
引言:胃壁增厚的影像学迷雾 在腹部增强CT检查中,胃壁的正常厚度通常不超过5毫米。当放射科医生在报告中写下“胃壁增厚”时,这个看似简单的描述,实际上打开了一扇通往复杂鉴别诊断的大门。胃壁增厚本身并非一种疾病,而是一个影像学征象,它像一道待解的谜题,其答案可能指向多种病理状态。常见的原因包括良性的慢性胃炎、胃溃疡,以及恶性的胃癌、胃间质瘤,也包括本文讨论的核心...
2026-04-10
-
尿血-无痛血尿当上火,泌尿外科膀胱镜发现菜花样肿物
引言:被忽视的健康警报 在日常生活中,许多人发现尿液颜色变红或呈洗肉水样时,第一反应常将其归咎于“上火”。尤其是在没有伴随疼痛、发热等明显不适的情况下,“不痛不痒,应该只是上火了”的想法更为普遍。这种基于民间经验的自我诊断,可能导致对潜在严重健康问题的延误。事实上,血尿,特别是无痛性肉眼血尿,是泌尿系统发出的重要警报信号,其背后可能隐藏着从感染、结石到肿瘤等...
2026-03-13
-
褪黑素-睡眠
在人类生命的三分之一时间里,我们处于睡眠状态。这一看似被动的过程,实则由一套精密的生物系统所驱动,其中,一种被称为“褪黑素”(Melatonin)的激素扮演着核心角色。它如同夜幕降临时悄然亮起的“信号灯”,向身体发出“准备入睡”的指令,协调着我们的昼夜节律与睡眠-觉醒周期。随着现代社会生活节奏加快、光污染加剧以及电子屏幕的普及,睡眠障碍已成为全球性的公共卫生...
2026-03-21
-
胸膜间皮瘤-石棉接触史胸水查不出原因,胸外科胸腔镜活检确诊
在呼吸科或胸外科门诊,我们有时会遇到这样一类患者:他们多为中老年男性,有明确的石棉接触史(可能是在数十年前的建筑、造船或矿业工作中),因逐渐加重的胸闷、气促和持续性胸痛前来就诊。胸部影像学检查,如X光或CT,往往提示存在中到大量的胸腔积液,即通常所说的“胸水”^。反复的胸腔穿刺抽液进行常规生化、细胞学检查,却常常回报为“未见恶性肿瘤细胞”或“渗出液,原因待查...
2026-03-07
-
雀斑-日晒部位褐色点,遗传
引言 在人类肌肤的“地图”上,雀斑是一种独特而普遍的景观。它们通常以针尖至米粒大小的黄褐色或淡褐色斑点形式,悄然分布在面部、鼻梁、双颊、手背等日光偏爱的区域。这些看似微小的印记,远非简单的皮肤瑕疵,而是个体遗传密码与自然环境——特别是紫外线——之间一场漫长而复杂的对话结果。本文旨在系统性地探讨雀斑的本质,从其定义与临床特征出发,深入剖析其形成的核心机制,即遗...
2026-04-25
-
细菌性痢疾-夏秋季腹泻,大便培养志贺菌
夏秋季腹泻的元凶:细菌性痢疾的病原诊断、流行特征与综合防治策略 引言:一种被低估的肠道威胁 夏秋之交,气温升高、湿度增大,各类肠道传染病进入高发期。在众多以腹泻为主要症状的疾病中,细菌性痢疾(简称菌痢)因其传染性强、临床表现典型且可能引发严重并发症,始终是公共卫生领域关注的重点。菌痢是由志贺菌属(俗称痢疾杆菌)引起的一种法定乙类肠道传染病,其典型特征为发热、...
2026-05-09
-
脊髓肿瘤-进行性下肢无力,感觉平面上升
脊髓肿瘤,作为发生于脊髓、脊膜或神经根上的占位性病变,其临床表现复杂且呈进行性发展,其中进行性加重的下肢无力与感觉平面上升是极具特征性的核心症状组合。这两个症状的出现与演变,深刻揭示了肿瘤对脊髓这一中枢神经传导通路压迫与损害的动态过程,是临床诊断与评估病情进展的关键线索。 一、 症状的病理生理学基础:脊髓结构与功能的破坏 脊髓是大脑与躯干、四肢之间感觉与运动...
2026-04-25
-
食管癌-食管癌术后只能吃流食,营养科医生说这样搭配不会营养不
精细喂养,强健体魄——食管癌术后流食期科学营养搭配全解析 引言:跨越进食困境,构筑营养基石 食管癌手术是治疗该疾病的重要手段,但术后往往伴随一个严峻的挑战:吞咽功能的重建与限制。在术后初期,为保护吻合口、减少消化道负担,医生通常会要求患者经历一段时间的“流食期”。对于患者和家属而言,“只能吃流食”常与“营养不足”、“身体虚弱”的担忧紧密相连。现代临床营养学的...
2026-03-23
-
血管炎-下肢紫癜当过敏性皮炎,皮肤科医生让查血发现血管炎
皮肤作为人体最大的器官,常常是内部疾病的“晴雨表”。当双下肢出现对称性、按压不褪色的紫红色瘀点或瘀斑时,最常见的初步诊断方向之一便是过敏性皮炎。 部分患者在接受常规抗过敏治疗后,皮疹不仅未见消退,甚至可能伴有新发的关节肿痛或腹痛,一个更深层、更系统性的疾病——血管炎,便可能隐藏在这片皮损的“迷雾”之后。 血管炎是一组以血管壁炎症和坏死为共同病理特征的异质性疾...
2026-03-31
-
脂联素-胰岛素敏感性
胰岛素抵抗是2型糖尿病、肥胖及代谢综合征等一系列重大代谢性疾病的共同病理生理基础,如何有效改善胰岛素敏感性已成为全球公共卫生领域的核心挑战。传统观点认为脂肪组织仅是能量储存的器官,然而近二十余年的研究彻底颠覆了这一认知,揭示脂肪组织是一个高度活跃的内分泌器官,能够分泌多种具有生物活性的脂肪因子,其中脂联素(Adiponectin, ADPN)因其卓越的胰岛素...
2026-03-19
-
纹身-外源性色素
引言:跨越千年的身体艺术与现代科学审视 纹身,作为一种古老的身体修饰艺术,其历史可追溯至数千年以前。从古埃及的祭祀符号到波利尼西亚部落的社会等级标识,再到当代流行文化中的个性表达,纹身始终承载着人类复杂的社会、文化与审美意涵。随着纹身在全球范围内的日益普及,其核心媒介——植入皮下的 外源性色素 ——的安全性、长期生物相容性及潜在健康风险,已成为医学、毒理学和...
2026-03-20
-
肝癌-手术切除了肝癌,五年没复发是不是就治愈了?肝胆外科医生
跨越五年里程碑:临床治愈与终身随访的辩证——一位肝胆外科医生的视角 引言:五年之期的希望与隐忧 “手术很成功,五年没复发,恭喜您!”在肝胆外科的诊室里,医生对复查结果良好的患者说出这句话时,总是带着由衷的喜悦。对于肝癌患者而言,术后五年无病生存是一个极具象征意义的胜利节点。大量临床数据表明,肝癌术后复发多集中在前三年,五年后复发概率会大幅下降。医学界普遍将“...
2026-03-09
-
血管性水肿-眼睑口唇肿胀,可伴喉头水肿
引言:一种突发的“面具”与潜在的风险 想象一下,一觉醒来,发现自己的眼皮肿得像核桃,嘴唇厚如香肠,皮肤紧绷发亮,却无明显痛痒。这并非电影特效,而是血管性水肿患者可能遭遇的真实场景。血管性水肿,也称为血管神经性水肿或巨大性荨麻疹,是一种因皮肤和黏膜深层小血管扩张、通透性增加,导致组织液快速积聚的局限性水肿^。它好发于皮下组织疏松的区域,眼睑、口唇、外生殖器是“...
2026-03-29
-
膀胱癌-膀胱癌电切术后反复复发,泌尿外科医生说这次要全切
——一名反复复发膀胱癌患者的治疗心路与医学反思 摘要 :膀胱癌,作为泌尿系统最常见的恶性肿瘤之一,其治疗与预后高度依赖于病理分期与分级。对于非肌层浸润性膀胱癌,经尿道膀胱肿瘤电切术(TURBT)是标准且保留器官的首选治疗方式。高复发率是其临床面临的主要挑战。本文通过构建一个虚构但基于典型临床案例的患者叙事,深度剖析膀胱癌患者在经历多次TURBT术后仍反复复发...
2026-03-07
-
淋巴结肿大-颈部淋巴结肿大切除后病理提示结核,不是肿瘤但也要
引言:从担忧肿瘤到确诊结核 颈部出现无痛性、进行性增大的肿块,是许多人就医的常见原因,其背后往往隐藏着对恶性肿瘤的深深忧虑。当患者经历检查、甚至手术切除活检后,病理报告上赫然写着“结核”而非“癌”时,一种复杂的情绪油然而生——既有对排除肿瘤的庆幸,也有对“结核”这一慢性传染病的陌生与不安。颈部淋巴结结核,作为最常见的肺外结核之一,其诊断过程本身就是一次关键的...
2026-03-13
-
肠结核-腹痛腹泻,肠镜见环形溃疡
一、 引言:被忽视的肠道感染 在全球范围内,结核病仍是严重的公共卫生问题。当人们将目光聚焦于肺结核时,肠道作为肺外结核最常见的感染部位之一,其重要性常被低估。肠结核起病隐匿,症状不典型,极易与炎症性肠病、肠道肿瘤等疾病混淆,导致误诊或延迟诊断。腹痛与腹泻作为其核心肠道症状,背后是结核分枝杆菌在肠壁淋巴组织中引发的复杂病理过程。而消化内镜,尤其是结肠镜的广泛应...
2026-04-11
-
过敏性紫癜-孩子腿上起红点当过敏,儿科医生说这是血管炎要查尿
引言:被误解的“红点”——从皮肤到系统的警报 孩子活泼好动,腿上突然出现一片片红色斑点,不痛不痒,这场景在许多家庭中都曾上演。多数家长会将其归咎于蚊虫叮咬、湿疹或食物过敏,采取外用药膏或抗过敏药物处理。若这些红点具有几个关键特征: 集中分布于双小腿、脚踝及臀部,且呈对称性;颜色为鲜红或紫红,微微凸起于皮肤;最关键的是,用手指按压后颜色不消退 ,那么,这极有可...
2026-03-29
-
间接胆红素-溶血
从溶血到黄疸:揭秘间接胆红素生成与代谢的失衡之路 摘要 :间接胆红素作为红细胞衰老破坏后的核心代谢产物,其血清水平的升高是临床评估溶血性疾病及肝脏功能状态的关键窗口。本文旨在系统阐述间接胆红素的生成机制,深入剖析溶血性黄疸发生的病理生理学基础,并梳理其病因、临床表现、诊断思路与管理策略,为理解这一常见生化指标异常背后的复杂临床图景提供全面视角。 一、 间接胆...
2026-05-07
-
雷诺现象-遇冷手指变白变紫
在日常生活中,我们偶尔会注意到自己或他人手指颜色在特定环境下发生奇异的变化:接触冷水、身处空调房或情绪激动时,指尖会突然失去血色,变得苍白如蜡,随后转为青紫,最终在恢复过程中呈现出异常的潮红,并伴有麻木、刺痛或灼热感。这并非简单的“冻僵”或“气血不足”,而是一种被称为雷诺现象(Raynaud‘s phenomenon)的临床综合征的典型表现。这种由肢端小动脉...
2026-03-20
-
脑转移癌-乳腺癌术后五年突然头痛呕吐,神经外科会诊发现脑转移
五年平稳期后的颅内警报:一例乳腺癌术后脑转移的深度剖析 摘要 :本文通过一例乳腺癌根治术后五年,以突发头痛、呕吐为首发症状,最终确诊为脑转移瘤的典型病例,系统梳理了乳腺癌脑转移的常见临床症状谱、病理生理机制、现代影像学与分子诊断方法,并探讨了以神经外科为主导的多学科综合治疗策略。文章强调,对于有乳腺癌病史的患者,即使术后多年,任何新发的神经系统症状都需高度警...
2026-03-07
-
血友病-孩子磕碰就关节肿胀,血液科医生说这是血友病,以后不能
引言:被“放大”的磕碰 在普通孩子的童年里,奔跑、打闹、摔倒、爬起,是再寻常不过的成长印记。一次小小的磕碰,或许只会带来短暂的哭闹和一块很快消散的淤青。对于血友病患儿及其家庭而言,一次看似微不足道的跌倒或碰撞,却可能引发一场漫长的“风暴”——关节迅速肿胀、疼痛难忍,甚至可能造成永久性的损伤。那句“以后不能摔跤”的医嘱,并非过度的保护,而是一道沉甸甸的生命警示...
2026-03-07
-
腺病毒感染-咽结膜热,游泳池传播
引言 在炎炎夏日,公共游泳池是大众消暑纳凉、锻炼身体的热门场所。这片碧波荡漾的水域在带来清凉与欢乐的也可能成为某些病原体传播的温床,其中,腺病毒及其引发的咽结膜热尤为值得关注。这种以发热、咽炎和急性结膜炎为典型三联征的急性上呼吸道感染,因其与游泳池环境的特殊关联,常被称为“泳池热”。本文将深入剖析腺病毒,特别是其导致咽结膜热的病原学特征、在游泳池环境中的传播...
2026-04-06
-
雀斑-遗传,日晒加重
第一章:雀斑的生物学本质与临床表现 雀斑(Ephelides)是一种常见的、主要分布于面部、颈部和手背等日光暴露区域的皮肤色素沉着性疾病。 其典型表现为直径1-5毫米的圆形、卵圆形或不规则形淡褐色至深褐色斑点,边界清晰,通常无自觉症状。 雀斑多在儿童期(5-12岁)开始显现,青春期时可能因激素变化而颜色加深、数量增多,成年后趋于稳定,但会随季节和日晒程度而变...
2026-04-07
-
补体缺陷-反复细菌感染,自身免疫病
在人体复杂的免疫防御网络中,补体系统扮演着一支古老而精密的“快速反应部队”角色。它由约30种血浆蛋白和膜蛋白组成,通过级联反应被精准触发,执行清除病原体、调理吞噬、介导炎症反应乃至直接溶解靶细胞等关键任务。这支系统的高效运作依赖于激活与抑制之间的微妙平衡,如同驾驶汽车需要精准地踩下油门与刹车。当编码这些蛋白的基因出现先天错误,即发生遗传性补体缺陷时,这套精密...
2026-03-28
-
腹痛-上腹痛当胃病治了三年,肝胆外科查出胆总管结石
引言:被忽视的“右上腹警报” 在消化系统疾病的诊疗中,上腹部疼痛是一种极为常见的症状,其病因复杂,从常见的功能性消化不良、慢性胃炎到更为严重的炎、胆道疾病皆有可能。正是这种“常见”,有时却成了掩盖真相的面纱。许多患者,包括本文所参考的案例,曾长期将源自胆道系统的疼痛误判为“胃病”,历经数年反复治疗却收效甚微,直至症状加剧或出现特异性表现,才在专科检查下揭开谜...
2026-03-07
-
脑源性神经营养因子- BDNF
大脑的守护者:脑源性神经营养因子(BDNF)的生理功能、病理意义与未来潜能 引言 在探索大脑奥秘的漫长旅程中,科学家们发现了一种对神经系统的发育、维持与修复至关重要的蛋白质——脑源性神经营养因子(Brain-derived neurotrophic factor, BDNF)。自1982年首次从猪脑中被分离鉴定以来,BDNF因其广泛而强大的生物学功能,被誉为...
2026-04-09
-
重症联合免疫缺陷-婴儿反复感染,T细胞B细胞缺乏
重症联合免疫缺陷病(SCID)是儿科领域最严重的原发性免疫缺陷病之一,以T淋巴细胞和/或B淋巴细胞的先天性、重度缺陷为特征,导致患儿几乎完全丧失适应性免疫功能。婴儿期是其典型发病窗口,临床表现为反复、严重、迁延不愈的感染,且对常规治疗效果不佳。本文旨在系统阐述SCID的免疫学发病机制、临床特征、诊断策略及管理原则,重点剖析其导致婴儿反复感染的病理生理基础,以...
2026-03-26
-
乳腺癌-洗澡自摸发现肿块,超声提示BI-RADS 4类
从“自摸发现”到“4类警示”:乳腺癌筛查与诊断的关键一步 引言:自我检查——不可替代的初级防线 乳腺癌是全球女性最常见的恶性肿瘤之一,其早期发现与及时治疗对预后至关重要。在专业筛查尚未普及或间隔期内,规律的自我检查(Breast Self-Examination, BSE)是一项简单、经济且有效的初级预警手段。据统计,约80%的乳腺癌最初是由患者自己发现的。...
2026-03-06
-
肿瘤标志物-筛查,随访
在癌症防控与管理的全链条中,早期发现与有效监测是改善预后的两大基石。肿瘤标志物检测,通过分析血液、体液等样本中由肿瘤细胞产生或机体应对肿瘤而异常改变的物质,为此提供了重要的辅助手段^。其在临床实践中主要扮演两大核心角色:一是作为面向特定高危人群的早期筛查“哨兵”,力图在症状出现前捕捉风险信号;二是作为已确诊患者的随访“导航仪”,用于评估疗效、预警复发及判断预...
2026-04-07
-
肝硬化-肝硬化腹水抽了又长,肝病科医生调了一个药,腹水慢慢消
肝硬化腹水,是失代偿期肝硬化患者常见的严重并发症。对于许多患者和家庭而言,那反复穿刺抽液、腹水“抽了又长”的循环,不仅是身体的沉重负担,更是精神上的无尽折磨。它像一个顽固的幽灵,盘踞在腹腔,消耗着患者的营养,压迫着脏器,限制着呼吸,并时刻预示着肝功能进一步恶化的风险。传统的治疗往往围绕利尿、限盐、补充白蛋白以及腹腔穿刺放液术(LVP)展开,对于难治性腹水患者...
2026-03-09
-
骨痛-全身骨痛当风湿治两年,骨科医生让查血发现多发瘤
在骨科或风湿免疫科门诊,因“全身骨痛”前来就诊的患者屡见不鲜。许多患者,尤其是中老年人,其疼痛常被初步归因于骨质疏松、骨关节炎或风湿性疾病,并接受相应的对症治疗。当疼痛持续不缓解、常规治疗无效时,一个更具侵袭性的病因——多发性瘤,便可能隐藏在表象之下。临床上,患者因骨痛被当作“风湿”治疗数月甚至数年,最终通过一次偶然或常规的血液检查发现异常指标,从而确诊为多...
2026-03-07
-
软下疳-外阴溃疡疼痛,链杆菌阳性
摘要 软下疳是一种由杜克雷嗜血杆菌(Haemophilus ducreyi)引起的经典性传播疾病,临床上以生殖器部位出现一个或多个疼痛性溃疡,并常伴发腹股沟淋巴结肿大、化脓及破溃为典型特征^。其病原体为一种革兰染色阴性的短棒状链杆菌,显微镜下可见其呈鱼群状排列,此特征是实验室诊断的重要依据^。本文旨在系统阐述软下疳的病原学、临床表现、诊断与鉴别诊断,重点围绕...
2026-04-29
-
透明细胞汗腺瘤-结节,大汗腺分化
透明细胞汗腺瘤:基于结节性生长与大汗腺分化的临床病理学解析 一、 引言与疾病概述 透明细胞汗腺瘤,亦称结节状汗腺瘤(Nodular Hidradenoma)或透明细胞肌上皮瘤,是一种起源于皮肤汗腺、通常表现为良性行为的附属器肿瘤。 其核心特征在于肿瘤在真皮内形成境界相对清楚的结节状结构,并且在组织学上常显示出向大汗腺(顶泌汗腺)分化的倾向。 尽管名称中含有“...
2026-04-16
-
T细胞淋巴瘤-皮肤红斑结节当湿疹,皮肤科医生让做病理
当“湿疹”久治不愈:皮肤红斑结节背后的T细胞淋巴瘤警讯 引言:皮肤上的“伪装者” 在皮肤科门诊,“湿疹”是一个极高频的诊断。它通常指向一组以红斑、丘疹、瘙痒、反复发作为特征的炎症性皮肤病。正是这种常见性,有时会成为某些严重疾病的“完美伪装”。当患者身上的“湿疹”表现为顽固的红斑、浸润性斑块或结节,且对常规治疗反应不佳时,一个危险的信号已然亮起——这可能是皮肤...
2026-03-06
-
隐孢子虫病-腹泻水样便,免疫功能低下
隐孢子虫病是由隐孢子虫属原虫引起的人兽共患寄生虫病。自20世纪后期被确认为人类重要致病原以来,其已成为全球范围内,尤其是发展中国家儿童腹泻和免疫缺陷者严重肠道感染的重要原因之一。该病主要通过粪-口途径传播,受污染的水源和食物是主要媒介。隐孢子虫卵囊对常规消毒剂(如氯)具有较强抵抗力,使其在环境中持久存在,易引发水源性暴发流行。感染后,临床表现的核心是腹泻,但...
2026-05-01
-
缺铁性贫血-女性缺铁性贫血补铁三个月没好转,消化科医生让查大
当补铁无效时,为何消化科医生总让你查大便?——揭秘缺铁性贫血背后的“隐形失血” 引言:补铁无效的困惑与隐忧 “我每天都在按时吃铁剂,猪肝、菠菜、红枣也没少吃,为什么三个月过去了,血红蛋白还是纹丝不动?”这不仅是许多缺铁性贫血患者,尤其是女性患者的共同困惑,更是一个不容忽视的健康警报。缺铁性贫血看似是“缺什么补什么”的简单逻辑,但当常规补铁治疗遭遇瓶颈时,往往...
2026-03-31
-
胃溃疡-胃溃疡反复发作,最后切胃的病人,术前问了医生一句话
引言:一道划破寂静的提问 手术室前的走廊,总弥漫着一种独特的寂静,那是消毒水气味与无声焦虑混合而成的氛围。就在这样的寂静即将被手术门开合声打破的前一刻,五十二岁的陈建国躺在移动病床上,突然伸手轻轻拉住了主刀医生李主任的白大褂袖口。这位与胃溃疡反复搏斗了将近二十年的老教师,用因紧张而略显干涩的嗓音,问出了盘旋在心头数月,或许更久的问题: “李主任,切了它,我就...
2026-03-07
-
低热-下午低热盗汗当感冒治,呼吸科医生让拍CT发现肺结核
午后低热与夜间盗汗:不容忽视的肺结核信号——从症状识别到CT诊断 引言 在呼吸系统疾病中,肺结核因其传染性和潜在的健康危害而备受关注。其早期症状常不典型,极易与普通感冒或上呼吸道感染混淆。许多患者因反复出现的午后低热、夜间盗汗等症状而自行服用感冒药,直至症状迁延不愈才前往医院,此时可能已错过了最佳干预时机。本文将深入剖析肺结核的典型与非典型症状,重点阐述“低...
2026-03-06
-
肾癌-无痛血尿两天自己好了,一年后腰痛查出肾癌,泌尿外科医生
引言:一个被忽视的“小插曲” 在泌尿外科的诊室里,张先生(化名)的故事并非个例。一年前,他曾有过连续两天的无痛性肉眼血尿,尿液呈淡红色,但身体没有任何不适。血尿自行消失后,他便将此事抛诸脑后,认为只是“上火”或偶然现象。一年后,持续的腰部钝痛让他再次走进医院,经过一系列检查,最终被诊断为肾癌。主治医生沉重地指出:“一年前那次无痛血尿,很可能就是肿瘤发出的第一...
2026-03-07
-
胰岛细胞瘤-低血糖发作意识不清,神经内科医生让查
从意识不清到探查:神经内科医生如何识别胰岛细胞瘤 引言 在神经内科门诊或急诊,接诊以“突发意识不清”、“行为异常”或“反应迟钝”为主诉的患者是常见情景。常规的诊疗思路会首先指向脑血管意外、癫痫、代谢性脑病或中枢神经系统感染等。有一类疾病的根源并不在大脑,而在腹腔深处的。胰岛细胞瘤,尤其是胰岛素瘤,因其过量分泌胰岛素导致严重、反复的低血糖,可直接引发显著的神经...
2026-04-19
-
囊肿-体检发现囊肿,看了三个专家说法不一,最后手术证实是黏液
在常规健康体检日益普及的今天,越来越多的人在毫无症状的情况下,通过腹部超声或CT扫描,意外发现了上的“小东西”——囊肿。这本应是健康预警的福音,却常常成为患者焦虑与困惑的开端。囊肿种类繁多,性质迥异,从完全良性、无需处理的浆液性囊腺瘤,到具有恶性潜能的黏液性囊腺瘤,其诊疗路径和预后天差地别。临床实践中,不同专家基于经验、对影像细节的解读侧重以及风险偏好的差异...
2026-03-06
-
麻风病-皮肤感觉障碍,外周神经粗大
麻风病,作为一种由麻风分枝杆菌引起的慢性传染病,其历史与人类文明交织,常被蒙上恐惧与误解的面纱。从现代医学视角审视,麻风病有其独特的病理轨迹与临床特征。其临床表现虽具多样性,但核心在于对皮肤与周围神经系统的选择性侵犯。其中, 皮肤感觉障碍 与 周围神经粗大 构成了麻风病最具特征性、也最常导致诊断与功能损害的两大核心症候群。理解这两种症状,不仅是识别这一“模仿...
2026-04-29
-
食管癌-吞咽梗阻感半年,胃镜发现食管全周狭窄
引言 食管癌是我国高发的消化道恶性肿瘤之一,其典型临床症状常表现为进行性吞咽困难、异物感及胸骨后疼痛。当患者出现长达半年的吞咽梗阻感,并通过胃镜检查发现食管全周性狭窄时,这通常提示病变已进入中晚期阶段,临床处理面临严峻挑战。全周性狭窄意味着肿瘤已沿食管壁环形浸润生长,严重阻碍食团通过,并显著影响患者的生活质量与营养状况。本文旨在系统阐述此类病例的病理机制、诊...
2026-03-07
-
肺癌-体检胸片正常,一年后咳血查出肺癌,影像科医生说胸片有盲
在众多令人扼腕的医疗叙事中,这样的情节反复上演:一位中年高管,生活自律,坚持每年参加公司组织的全面体检,报告上“胸片未见异常”的字样年复一年,让他对自身健康充满信心。某一天,持续的干咳或痰中偶然出现的血丝打破了平静,进一步的CT检查结果却如晴天霹雳——肺癌,且已非早期。当事人与家属的困惑与震惊无以复加:“明明年年体检都正常,怎么会突然得癌,还是晚期?”类似的...
2026-03-07
-
艾滋病-发热腹泻体重下降,CD4下降
发热、腹泻、体重下降与CD4下降:艾滋病消耗综合征的深度解析 摘要 获得性免疫缺陷综合征(AIDS,艾滋病)是由人类免疫缺陷病毒(HIV)感染引起的慢性传染病。其疾病进展的核心标志是CD4+T淋巴细胞的进行性减少,导致免疫系统功能严重缺陷。当进入艾滋病期,患者常出现一系列消耗性症状,其中以持续发热、慢性腹泻和不明原因的显著体重下降最为典型,这三者常被统称为“...
2026-04-25
-
鞭虫病-慢性腹泻,大便鞭虫卵
本文旨在系统探讨由毛首鞭形线虫(鞭虫)感染引起的慢性腹泻的病因学、病理生理机制、临床表现、诊断方法及综合防治策略。文章首先概述鞭虫的生活史与感染途径,继而深入分析其导致肠道慢性炎症、黏膜损伤及功能紊乱的病理过程,详细阐述由此引发的慢性腹泻的临床特点与并发症。结合现有医学证据,提出诊断、治疗及预防的一体化方案,以期为临床实践和公共卫生干预提供参考。 一、 引言...
2026-03-27
-
肝转移癌-肠癌肝转移不能手术,介入科医生说可以先把肝脏血管堵
结直肠癌是全球范围内高发的恶性肿瘤,肝脏是其最常见的远处转移部位。一旦发生肝转移,疾病即进入IV期,传统的治疗观念曾一度将其视为难以治愈的晚期状态。外科手术切除虽是可能实现根治的手段,但仅有约20%-30%的患者在初诊时具备手术条件,多数患者因转移灶数量多、分布广、位置特殊或合并肝功能储备不足等原因,失去了根治性手术的机会。面对这一困局,以肝动脉化疗栓塞为代...
2026-04-14
-
尿痛-尿痛当尿路感染治了半年,妇科医生发现是间质性膀胱炎
在泌尿外科与妇科门诊,一种常被忽视的慢性疼痛症候群——间质性膀胱炎/膀胱疼痛综合征(IC/BPS),正让无数患者陷入漫长的诊疗迷途。患者常因尿频、尿急、下腹或盆腔疼痛就诊,其症状与普通尿路感染(UTI)高度相似,导致许多人在数月甚至数年间反复被当作“细菌性膀胱炎”治疗,服用大量抗生素却收效甚微,身心备受煎熬^。本文通过剖析一例典型误诊案例,深入探讨间质性膀胱...
2026-03-14
-
食欲肽- orexin
食欲肽-orexin:连接睡眠、能量稳态与神经疾病的关键神经肽系统 摘要 食欲肽(Orexin),亦称为下丘脑泌素(Hypocretin),是一对由下丘脑外侧区(Lateral Hypothalamus, LH)和穹窿周区(Perifornical Area, PFA)神经元合成和分泌的神经肽。自1998年被两个独立研究小组几乎同时发现以来,其在调控睡眠-觉...
2026-03-22
-
表皮生长因子- EGF
微观世界的生命建筑师:表皮生长因子(EGF)的发现、机制与未来 引言 在生命科学波澜壮阔的画卷中,一些微观分子因其卓越的调控能力而成为璀璨的明星,表皮生长因子(Epidermal Growth Factor, EGF)便是其中之一。自其被发现以来,EGF不仅深刻改变了我们对细胞生长、发育与修复的认知,更架起了从基础研究通往临床医学与生物技术应用的桥梁。这篇综...
2026-04-08
-
静脉性溃疡-小腿内侧淤积性皮炎,溃疡
在慢性伤口领域,下肢静脉性溃疡是一个沉重且普遍的健康负担,其人群发病率约为0.4%至1.3%,这意味着平均每百人中即有一人受累,在老年群体中比例更高。它常始于不起眼的皮肤瘙痒与色素沉着,最终可能演变为经年不愈的“老烂腿”,严重侵蚀患者的生活质量。这一病理链条的起点,往往正是小腿内侧的淤积性皮炎。淤积性皮炎,又称静脉曲张性湿疹,是静脉功能不全最具代表性的皮肤标...
2026-03-31
-
肺结核-咳血胸痛,胸片空洞,痰涂片阳性
引言:一例典型病例的启示 深夜的急诊室,一位38岁的男性患者被轮椅推进来,他面容憔悴,以手捂胸,伴随着阵阵压抑的咳嗽。当护理垫递到他面前时,他咳出数口鲜红色、混有泡沫的痰液——这是典型的“咳血”(咯血)。他自述近两个月来反复午后低热、夜间盗汗、体重明显下降,近一周胸痛加剧,尤以深呼吸和咳嗽时为甚。这组症状组合—— 慢性消耗性症状(发热、盗汗、消瘦) 加上 呼...
2026-04-14
-
色素痣-黑色素细胞增生
色素痣,俗称“痣”或“黑痣”,几乎是每个人皮肤上都存在的“印记”。它们或大或小,或平或凸,颜色深浅不一,是皮肤最常见的良性肿瘤之一。尽管多数色素痣终身无害,但其形成机制、类型区分以及与恶性黑色素瘤的潜在关联,始终是公众关注和医学研究的重点。本文旨在系统阐述色素痣的本质——黑色素细胞的良性增生,深入剖析其成因、分类、临床特征、诊断方法及科学管理策略,以期为读者...
2026-04-18
-
肺腺癌-女性不吸烟肺腺癌,基因检测发现EGFR突变,靶向药有
在肺癌的诸多亚型中,肺腺癌在女性、不吸烟人群中的发病率尤为突出,其分子生物学特征也呈现出鲜明的独特性。其中,表皮生长因子受体(EGFR)基因突变是驱动肿瘤发生、发展的关键分子事件,并为靶向治疗提供了精准的“打击靶点”。这一发现彻底改变了此类患者的治疗格局,使得以口服靶向药物为代表的精准医疗成为一线标准选择。本文将围绕女性不吸烟肺腺癌患者EGFR突变的流行病学...
2026-04-19
-
乙肝-家里有乙肝患者一起吃饭会传染吗?传染科医生说先看对方有
引言:被误解的日常接触 在中国,乙型肝炎病毒(HBV)感染是一个备受关注的公共卫生议题,同时也承载了沉重的社会污名。其中,一个普遍且根深蒂固的担忧是:“家里有乙肝患者,一起吃饭会传染吗?”这个问题背后,折射出公众对乙肝传播途径的模糊认知与无端恐惧,常常导致不必要的家庭隔阂与社会歧视。本文将基于可靠的医学证据,系统阐述乙肝病毒的传播机制,明确日常共餐的真实风险...
2026-03-06
-
血小板衍生生长因子- PDGF
血小板衍生生长因子(PDGF):从基础生物学到临床转化的多维视角 摘要 血小板衍生生长因子(Platelet-Derived Growth Factor, PDGF)是一类重要的多效性细胞因子,自被发现以来,其在细胞增殖、迁移、分化及组织修复等基本生命过程中的核心作用不断被揭示。本文旨在系统综述PDGF家族成员及其受体的分子结构与遗传学特征,详细阐述其介导的...
2026-04-09
-
腹水-肚子越来越大以为是长胖,消化科医生叩诊发现移动性浊音
当“发福”的肚子遇上医生的叩诊锤:一位消化科医生的诊断手记 引言:被误读的“福态” 在消化科门诊,我时常会遇到一些面露困惑与些许尴尬的患者,他们最常见的开场白是:“医生,我最近好像胖得特别快,尤其是肚子,可人却没精神,吃不下饭。” 张先生便是其中一位。他五十出头,事业有成,自述近半年来腹部逐渐膨隆,起初以为是应酬多、运动少导致的“啤酒肚”,尝试过节食和健身,...
2026-03-07
-
溶血性贫血-酱油色尿当血尿,肾内科医生说可能是溶血
在临床诊疗中,尿液颜色是反映机体健康状况的重要窗口之一。正常尿液呈淡黄色至琥珀色,其深浅主要取决于尿色素浓度和饮水量的多寡。当尿液呈现异常的“酱油色”或“浓茶色”时,这往往是一个需要高度警惕的信号。患者常因此惊慌,首先联想到的便是“血尿”。诚然,泌尿系统疾病是导致血尿的常见原因,但并非所有深色尿液都意味着红细胞直接漏入尿路。在肾内科及血液科领域,一种需要仔细...
2026-03-12
-
钩虫病-贫血异食癖,大便找钩虫卵
在寄生虫病的谱系中,钩虫病以其独特的“吸血”方式和对宿主健康的渐进性损害而著称。其成虫体长约1厘米,前端具有发达的口囊,内藏钩齿或板齿,使其能够牢牢吸附于宿主的小肠黏膜上。这种看似微小的生物,通过长期的、隐匿的血液掠夺,最终导致宿主出现以贫血为核心的一系列临床症状,严重者甚至危及生命。而伴随重度贫血出现的异食癖,更是为这种疾病增添了一层神秘的病理色彩。临床诊...
2026-05-01
-
肝转移癌-肠癌术后三年肝上发现占位,肝胆外科评估后二次手术切
引言:当转移的阴影再次降临 对于许多结直肠癌患者而言,成功完成初次根治性手术,意味着赢得了一场至关重要的战役。术后的康复之路并非总是一帆风顺。据统计,高达50%至70%的结直肠癌患者在术后会出现肝转移,其中一部分甚至在术后三年内,于定期复查中发现肝脏出现了新的“占位性病变”。这无疑是给患者和家庭投下的一片沉重阴影。当影像报告上出现“肝内多发占位,考虑转移瘤可...
2026-03-08
-
软骨样汗管瘤-汗腺肿瘤
摘要 软骨样汗管瘤,亦称皮肤混合瘤,是一种起源于汗腺、临床上较为罕见的良性皮肤附属器肿瘤。其病理学特征为上皮细胞与间质成分(尤其是软骨样基质)的混合性增生,形态多样,易与其他皮肤肿瘤混淆。本文旨在系统阐述软骨样汗管瘤的流行病学特征、病因与发病机制、临床病理学特点、诊断与鉴别诊断、治疗策略及预后,以期为临床医生与病理科医师提供全面的参考,促进对此类疾病的认识与...
2026-04-15
-
视黄醇结合蛋白4-胰岛素抵抗
视黄醇结合蛋白4(Retinol-Binding Protein 4, RBP4)长期以来被认为是负责在血液中特异性转运维生素A(全反式视黄醇)的主要载体蛋白,对于维持视觉、免疫及上皮组织健康至关重要。自21世纪初以来,一系列突破性研究揭示了RBP4的另一重关键身份:一种由脂肪组织分泌的脂肪因子,其在肥胖、2型糖尿病、代谢综合征等疾病的胰岛素抵抗发生发展中扮...
2026-03-19
-
胼胝-足底弥漫性角化,摩擦引起
引言 在我们的日常生活中,足底皮肤变硬、增厚形成俗称的“老茧”,是一种极为普遍的现象。这种看似微不足道的皮肤变化,实则是人体应对长期机械刺激的一种复杂而精妙的保护性反应。当这种角质增厚超出正常生理范畴,或与特定病理状态相结合时,便会演变为困扰人们行走、影响生活质量的足部问题。其中,由长期摩擦压迫引起的胼胝(callus)与具有遗传背景的弥漫性掌跖角化病(di...
2026-03-31
-
胃癌-年轻女性贫血多年,胃镜发现皮革胃
被贫血掩盖的胃之“铠甲”:一例年轻女性皮革胃的深度启示 引言:当贫血成为“报警信号” 在临床实践中,年轻女性出现慢性贫血是一个常见但原因复杂的征象。它可能源于营养因素、月经过多、血液系统疾病,亦可能是一些隐匿性慢性失血或消耗性疾病的外在表现。其中,消化道肿瘤,尤其是胃癌,因其典型症状如腹痛、黑便、消瘦等更易被警惕,但对于一种特殊类型的胃癌——“皮革胃”而言,...
2026-05-01
-
视黄醇结合蛋白-营养,肾功
视黄醇结合蛋白:营养状况的“晴雨表”与肾脏健康的“微观哨兵” 在临床医学与健康评估的精密图谱中,诸多生物标志物如同功能各异的“侦察兵”,为洞察机体内部的微妙变化提供关键线索。其中,视黄醇结合蛋白(Retinol-Binding Protein, RBP)作为一种由肝脏合成的小分子蛋白质,正日益凸显其超越单一维度的复合价值。它不仅是维生素A(视黄醇)在血液中的...
2026-03-18
-
肠病性关节炎-炎症性肠病伴关节炎
在临床医学的交叉地带,存在着一类常被忽视却严重影响患者生活质量的疾病——肠病性关节炎,尤其是与炎症性肠病(Inflammatory Bowel Disease, IBD)伴发的关节炎。这是一种典型的“肠-关节”共病现象,指由克罗恩病(Crohn‘s Disease, CD)或溃疡性结肠炎(Ulcerative Colitis, UC)等慢性肠道炎症性疾病引发...
2026-03-25
-
食管癌-吃东西总觉得噎得慌,做了胃镜没事,半年后确诊食管癌
引言:一个常见的症状与一次“安心”的检查 在消化内科门诊,患者主诉“吃东西总觉得噎得慌”是极为常见的现象。这种吞咽时的哽噎感,医学上称为“吞咽困难”或“吞咽不适”,其背后原因多样,从良性的功能紊乱到严重的器质性病变皆有可能。对于这一症状,胃镜检查(食管胃十二指肠镜检查)被公认为评估上消化道、尤其是食管黏膜状况的“金标准”。它能直接观察食管内壁,发现炎症、溃疡...
2026-03-07
-
胆碱酯酶-肝合成功能
在常规的肝功能检查中,转氨酶(ALT/AST)因其与肝细胞损伤的直接关联而备受关注,常被视为肝脏健康的“警报器”。另一项同样由肝脏独家制造、默默反映着肝脏根本“生产力”的指标—— 血清胆碱酯酶 ,其临床价值却常被忽视。胆碱酯酶并非肝脏损伤的“事后报告者”,而是肝脏合成储备功能的“实时监测仪”与“实力储备卡”。它如同一座化工厂的产能表,直观地展示着肝脏这台精密...
2026-04-08
-
夜尿多-夜尿三四次当肾虚,泌尿外科查出前列腺增生压迫尿道
夜间睡眠时起床排尿超过2次,医学上称为夜尿症。这一症状严重影响睡眠质量和日间精神状态,长期如此还可能诱发焦虑、抑郁等心理问题,并增加跌倒风险。当症状出现,尤其在中老年男性群体中,一个普遍存在的认知误区是将其归因于“肾虚”。中医理论中的“肾虚”确实可能包含夜尿频多,尤其是肾阳虚或肾气虚时,常伴腰膝酸软、畏寒怕冷等症状。现代医学研究表明,夜尿增多是一个多因素症状...
2026-03-06
-
肾状癌-多房囊性肾占位,手术病理状癌
肾状癌的多房囊性占位表现:从影像特征到病理诊断与临床管理 引言 肾脏囊性占位性病变在临床影像学检查中颇为常见,其诊断与鉴别诊断一直是泌尿外科与影像科的挑战。其中,多房囊性肾占位,尤其是当病理诊断为肾状癌时,构成了一个独特的亚群。肾状癌作为肾细胞癌(RCC)的第二常见亚型,约占肾癌病例的10%至15%。虽然典型的肾状癌在影像上多表现为实性肿块,但有相当一部分,...
2026-04-23
-
荨麻疹-风团,24小时内消退
皮肤上突然涌现一片片红色或苍白的隆起,伴随难以忍受的瘙痒,却在数小时内悄然隐退,不留一丝痕迹——这便是荨麻疹,一种常见的过敏性皮肤病。其最核心、最典型的临床表现,即是被称为“风团”的皮损。风团“突发突消”的特性,尤其是其通常在24小时内自行消退的规律,不仅是患者最直观的感受,更是临床医生进行诊断、鉴别和制定管理策略的关键依据。这一看似简单的生理现象,背后却蕴...
2026-04-15
-
胸痛-胸痛当心绞痛治了半年,做了一次胃镜发现是反流性食管炎
胸痛半年,误当心绞痛?——反流性食管炎的诊断迷雾与破局之道 在急诊科与心内科门诊,胸痛是最常见的主诉之一,其背后病因复杂,从危及生命的心肌梗死到相对“温和”的消化系统疾病,谱系广泛。临床上,有一种胸痛极具迷惑性,它发作时酷似心绞痛,让患者辗转心内科数月甚至更久,反复进行心脏检查却始终未果,直到一次胃镜检查才揭晓谜底——反流性食管炎。本文旨在深入剖析这种以胸痛...
2026-03-07
-
非淋菌性尿道炎-尿道刺痒稀薄分泌物,衣原体阳性
非淋菌性尿道炎(Nongonococcal Urethritis, NGU)是临床上最常见的性传播疾病之一,其特点是在尿道炎症状的患者中,无法检测到淋球菌。 在NGU的病原谱中,沙眼衣原体(Chlamydia trachomatis)是首要的致病元凶,约占病例的40%-50%,其次为解脲支原体(Ureaplasma urealyticum)等。 衣原体是一种...
2026-04-28
-
乳腺癌-丈夫陪妻子做乳腺检查,自己顺便查了一下,结果查出乳腺
当“她”的疾病降临于“他”:一次乳腺检查引发的生命警示与思考 ——从一个“顺便检查”的真实故事说起 引言:一次“无心插柳”的检查,揭开被忽视的真相 在大多数人的认知图谱中,“乳腺癌”与女性形象紧密绑定,如同一个性别专属的标签。粉红丝带、女性健康月、针对女性的筛查宣传……这一切都构成了我们对这种疾病的主流叙事。一个看似偶然的事件,却像一枚投入平静湖面的石子,打...
2026-03-06
-
肾素-高血压
高血压是全球范围内最常见的慢性疾病之一,是心脑血管事件、肾脏疾病及死亡的主要危险因素。其发病机制复杂,涉及遗传、环境、神经内分泌等多重因素。其中,肾素-血管紧张素系统(Renin-Angiotensin System, RAS)作为体内关键的血压与体液平衡调节系统,在高血压尤其是继发性高血压及部分原发性高血压的发病中占据核心地位。肾素作为该系统的启动酶,其分...
2026-03-23
-
药物性红斑狼疮-药物诱发,抗组蛋白抗体
药物性红斑狼疮是指由服用特定药物后诱发产生的、临床表现与系统性红斑狼疮相似的自身免疫综合征。 其核心特征在于,通常在停用致病药物后,临床症状和实验室指标可得到缓解或消失,这与病因不明的特发性SLE形成重要区别。 在众多实验室指标中,抗组蛋白抗体(AHA)的阳性检出是DILE一个突出且常见的血清学特征。 组蛋白是细胞核内负责包装DNA的碱性蛋白质,抗组蛋白抗体...
2026-03-20
-
黑色素聚集激素- MCH
一、 引言:从鱼类色素调节到哺乳动物中枢的“多面手” 黑色素聚集激素(MCH)最初因其在硬骨鱼类中调节皮肤色素细胞、使黑色素颗粒聚集以应环境变化的功能而被命名和认识。这一发现揭示了其在进化上的保守性。随后的研究证实,在哺乳动物中,MCH主要由下丘脑外侧区(LHA)和未定带的神经元合成与分泌,其表达和功能发生了显著扩展,成为中枢神经系统中一个举足轻重的信号分子...
2026-03-21
-
肢端早老症-四肢皮肤早老
肢端早老症:聚焦四肢皮肤早老的病理机制与临床管理 摘要 肢端早老症(Acrogeria)是一种罕见的遗传性或获得性皮肤疾病,其核心特征为四肢末端(手、足)皮肤出现显著的、与年龄不相符的早老性改变,表现为皮肤非薄、萎缩、干燥、皱纹加深、皮下脂肪与软组织减少,并常伴有毛细血管扩张与色素异常。本文旨在系统综述肢端早老症的临床分型、流行病学、病因与发病机制(重点探讨...
2026-05-07
-
髓母细胞瘤-小脑蚓部占位,儿童后颅窝肿瘤
引言:被忽视的儿童颅内“隐形杀手” 在儿童恶性肿瘤的谱系中,脑肿瘤是仅次于白血病的第二大常见肿瘤,其中后颅窝是儿童颅内肿瘤最常发生的部位之一。而后颅窝肿瘤中,髓母细胞瘤(Medulloblastoma, MB)因其恶性程度高、进展迅速,成为备受关注的“儿童杀手”。它主要起源于小脑蚓部,即位于后颅窝中线、协调身体平衡与精细运动的关键区域。由于其早期症状如头痛、...
2026-04-06