-
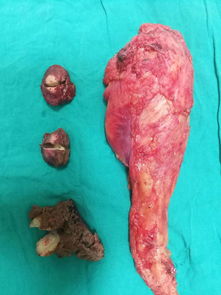
隆凸性皮肤纤维肉瘤-躯干结节,局部复发
隆突性皮肤纤维肉瘤(Dermatofibrosarcoma Protuberans, DFSP)是一种起源于皮肤纤维组织的低度恶性肿瘤。尽管其远处转移率相对较低(通常不足5%),但其局部侵袭性强,术后具有较高的局部复发倾向,构成了临床诊疗中的核心挑战。该肿瘤好发于躯干和四肢近端,其中躯干是最常见的发病部位。患者通常为青壮年,男性发病率可能略高于女性。本文旨在...
2026-04-26
-
血钙-高钙低钙
引言 钙离子是人体内含量最丰富的矿物元素,在维持神经肌肉兴奋性、信号传导、骨骼健康、血液凝固以及酶活性调节等方面发挥着至关重要的作用。血钙,即血清中的钙浓度,其稳定是机体生命活动正常进行的基本保障。血钙稳态由甲状旁腺激素(PTH)、活性维生素D(1,25-(OH)2D3)和降钙素(CT)三者构成的精密内分泌网络共同调节,主要涉及肠道吸收、骨骼储存与释放以及肾...
2026-04-05
-
血小板活化因子- PAF
血小板活化因子:一种多功能磷脂介质的生物学特性与病理生理意义 摘要 血小板活化因子(Platelet-Activating Factor, PAF)是一种具有强大生物活性的磷脂类介质,化学名称为1-O-烷基-2-乙酰基-sn-甘油-3-磷酸胆碱。自1972年被发现并以其激活血小板的能力命名以来,PAF的研究已远远超出了血液学的范畴。本文旨在系统综述PAF的合...
2026-03-23
-
血管紧张素-血管收缩
血管紧张素:血管收缩的核心调控者及其在心血管健康中的双重角色 在人体复杂而精密的生理调控网络中,血压的稳定是维持生命活动的基础。其中,肾素-血管紧张素系统扮演着至关重要的角色,而血管紧张素,尤其是其活性形式血管紧张素II,则是这一系统的核心效应分子,通过引发血管收缩这一关键生理反应,对血压和体液平衡进行精细调节。血管收缩不仅是机体应对急性失血等紧急状况的救命...
2026-04-29
-
乳腺癌-洗澡自摸发现肿块,超声提示BI-RADS 4类
从“自摸发现”到“4类警示”:乳腺癌筛查与诊断的关键一步 引言:自我检查——不可替代的初级防线 乳腺癌是全球女性最常见的恶性肿瘤之一,其早期发现与及时治疗对预后至关重要。在专业筛查尚未普及或间隔期内,规律的自我检查(Breast Self-Examination, BSE)是一项简单、经济且有效的初级预警手段。据统计,约80%的乳腺癌最初是由患者自己发现的。...
2026-03-06
-
脑啡肽-镇痛
疼痛,作为人类最古老、最原始的体验之一,既是身体损伤的警报系统,也是折磨无数患者的沉重枷锁。在人类与疼痛的漫长斗争中,从草药到,从物理疗法到神经外科手术,止痛方式不断演进。最精妙、最根本的镇痛系统,恰恰隐藏在我们自身之内——内源性系统。其中,脑啡肽作为该系统的重要成员,自1975年被发现以来,便如同一把关键的钥匙,为我们打开了理解“内在止痛”机制的大门。它不...
2026-03-22
-
囊肿-体检发现囊肿,看了三个专家说法不一,最后手术证实是黏液
在常规健康体检日益普及的今天,越来越多的人在毫无症状的情况下,通过腹部超声或CT扫描,意外发现了上的“小东西”——囊肿。这本应是健康预警的福音,却常常成为患者焦虑与困惑的开端。囊肿种类繁多,性质迥异,从完全良性、无需处理的浆液性囊腺瘤,到具有恶性潜能的黏液性囊腺瘤,其诊疗路径和预后天差地别。临床实践中,不同专家基于经验、对影像细节的解读侧重以及风险偏好的差异...
2026-03-06
-
肾状癌-多房囊性肾占位,手术病理状癌
肾状癌的多房囊性占位表现:从影像特征到病理诊断与临床管理 引言 肾脏囊性占位性病变在临床影像学检查中颇为常见,其诊断与鉴别诊断一直是泌尿外科与影像科的挑战。其中,多房囊性肾占位,尤其是当病理诊断为肾状癌时,构成了一个独特的亚群。肾状癌作为肾细胞癌(RCC)的第二常见亚型,约占肾癌病例的10%至15%。虽然典型的肾状癌在影像上多表现为实性肿块,但有相当一部分,...
2026-04-23
-
肺癌-体检胸片正常,一年后咳血查出肺癌,影像科医生说胸片有盲
在众多令人扼腕的医疗叙事中,这样的情节反复上演:一位中年高管,生活自律,坚持每年参加公司组织的全面体检,报告上“胸片未见异常”的字样年复一年,让他对自身健康充满信心。某一天,持续的干咳或痰中偶然出现的血丝打破了平静,进一步的CT检查结果却如晴天霹雳——肺癌,且已非早期。当事人与家属的困惑与震惊无以复加:“明明年年体检都正常,怎么会突然得癌,还是晚期?”类似的...
2026-03-07
-
结核病-咳嗽低热盗汗,抗感染无效,PPD强阳性
结核病,这一与人类历史纠缠数千年的古老疾病,至今仍是全球重大的公共卫生挑战。其病原体——结核分枝杆菌,以其顽强的生存能力和复杂的致病机制,持续威胁着人类健康。临床上,当患者出现 长期咳嗽、午后低热、夜间盗汗 这一经典“三联征”,且常规 抗感染治疗无效 时,结核病的可能性便急剧升高。若此时 结核菌素纯蛋白衍生物(PPD)试验呈现强阳性 反应,则犹如一张清晰的“...
2026-04-19
-
黑便-黑便一个月当胃出血治,输血后血色素不升,血液科医生让查
在临床实践中,消化道出血,尤其是表现为黑便的上消化道出血,是一类常见且紧急的病症。其标准诊疗路径通常围绕止血、补液、输血以及通过内镜等手段明确并处理出血灶展开。当患者遵循这一路径接受治疗后,若关键指标——如血红蛋白(血色素)——未能如期回升,这便构成了一个极具警示意义的临床“转折点”。它像一盏红灯,提示着初始诊断可能存在局限,或病情背后隐藏着更为复杂的病理生...
2026-04-20
-
视黄醇结合蛋白-营养,肾功
视黄醇结合蛋白:营养状况的“晴雨表”与肾脏健康的“微观哨兵” 在临床医学与健康评估的精密图谱中,诸多生物标志物如同功能各异的“侦察兵”,为洞察机体内部的微妙变化提供关键线索。其中,视黄醇结合蛋白(Retinol-Binding Protein, RBP)作为一种由肝脏合成的小分子蛋白质,正日益凸显其超越单一维度的复合价值。它不仅是维生素A(视黄醇)在血液中的...
2026-03-18
-
肝细胞癌-甲胎蛋白正常也不能排除肝癌,肝胆外科医生说B超有结
肝脏,被誉为人体最“沉默”的器官,因其强大的代偿功能,早期病变往往缺乏特异性症状。肝细胞癌(HCC)作为我国高发的恶性肿瘤之一,其预后与诊断时机密切相关。早期肝癌经有效治疗,五年生存率可显著提高,而一旦进入中晚期,治疗选择有限,预后往往较差。肝癌的早期筛查与精准诊断显得至关重要。在临床实践中,血清甲胎蛋白检测和肝脏B超检查构成了筛查的两大基石。公众乃至部分非...
2026-03-09
-
癌-洗澡摸到硬块不痛不痒,泌尿外科医生:这种最危险
警惕无痛之“石”——洗澡摸到硬块不可掉以轻心 在淋浴时的一次偶然触摸,可能会让许多男性心中一紧:上出现了一个硬块,却不痛不痒。这种“静默”的异常,因其缺乏典型疼痛信号的警示,反而在泌尿外科医生眼中,可能意味着更高的风险,尤其需要警惕恶性肿瘤的可能性。本文旨在系统梳理这一症状背后的成因、评估方法及应对策略,帮助公众科学认识,避免延误诊治。 一、 症状解读:为何...
2026-03-12
-
足菌肿-足部肿胀窦道,颗粒状物排出
引言 在热带与亚热带地区的田野乡间,一种缓慢侵蚀劳动者足部的疾病,因其初期的隐匿性与进展的慢性,常被忽视,直至导致严重的功能障碍与畸形。这便是足菌肿,一种由真菌或放线菌引起的慢性、化脓性肉芽肿性疾病。它以足部肿胀、窦道形成和排出特征性的颗粒状分泌物为核心临床三联征,给患者带来长期的痛苦与沉重的社会负担。本文旨在系统阐述足菌肿的病因学、临床表现、诊断策略及治疗...
2026-04-28
-
食管鳞癌-饮酒抽烟多年,食管中段鳞癌
食管癌是全球范围内常见的消化道恶性肿瘤,严重威胁人类生命健康。其中,食管鳞状细胞癌(Esophageal Squamous Cell Carcinoma, ESCC)是食管癌最主要的病理类型,在中国等地区高发。流行病学调查与临床研究反复证实,长期吸烟与过量饮酒是导致食管鳞癌,尤其是胸中段食管鳞癌的两个极为关键且相互协同的危险因素。本文旨在深入剖析吸烟、饮酒与...
2026-04-22
-
肠癌-便血以为是痔疮拖了一年,肛肠科医生指检后说:你早该来
副标题: 当习惯性自诊遇上生命警报,一位肠癌患者的迟来忏悔 一、 序幕:那一抹刺目的红 记忆里,第一次发现便血,是在去年初春。卫生间昏黄的灯光下,白色陶瓷上那几点嫣红,格外刺眼。心里“咯噔”了一下,但随即,一个声音迅速而熟练地安抚了我:“肯定是痔疮,老毛病了,最近火锅吃多了,熬夜上火了。” 这声音如此笃定,源于我,也源于我们许多人共同拥有的“医学常识”——便...
2026-03-08
-
血清蛋白电泳- M蛋白
血清,作为人体内环境的微观缩影,蕴含着数以千计的蛋白质,它们如同维持生命运行的精密元件,执行着运输、免疫、催化、信号传递等关键功能。当疾病来袭,特别是某些恶性增殖性疾病发生时,血清蛋白质的组成与比例会发生特征性的改变。血清蛋白电泳(Serum Protein Electrophoresis, SPE)正是绘制这份“蛋白质身份图谱”的核心技术。它如同一台精密的...
2026-05-07
-
骨肉瘤-骨肉瘤保肢手术还是截肢,骨科医生说功能比外观重要
功能优先:在骨肉瘤治疗中,为何“能用”比“好看”更重要 引言:从“保命”到“保命且保肢”的范式转变 骨肉瘤,一种好发于青少年的高度恶性肿瘤,曾因其凶险的预后和高死亡率,让截肢一度成为标准治疗方案。过去几十年来,以新辅助化疗、影像学精准评估和先进重建技术为支柱的综合治疗模式,彻底改变了这一疾病的治疗格局。如今,约80%-90%的肢体骨肉瘤患者有机会接受保肢手术...
2026-03-29
-
间接胆红素-溶血
从溶血到黄疸:揭秘间接胆红素生成与代谢的失衡之路 摘要 :间接胆红素作为红细胞衰老破坏后的核心代谢产物,其血清水平的升高是临床评估溶血性疾病及肝脏功能状态的关键窗口。本文旨在系统阐述间接胆红素的生成机制,深入剖析溶血性黄疸发生的病理生理学基础,并梳理其病因、临床表现、诊断思路与管理策略,为理解这一常见生化指标异常背后的复杂临床图景提供全面视角。 一、 间接胆...
2026-05-07
-
纤维肉瘤-躯干软组织肿块,病理梭形细胞
纤维肉瘤是一种起源于成纤维细胞的恶性肿瘤,属于软组织肉瘤的一种。其典型特征是肿瘤由形态一致的梭形细胞构成,这些细胞在显微镜下呈细长的纺锤状。梭形细胞肿瘤是一个涵盖良恶性病变的大家族,而纤维肉瘤是其中具有代表性的恶性成员。过去几十年,随着诊断技术的精进,一些过去被归类为纤维肉瘤的肿瘤被重新划入其他类型(如恶性纤维组织细胞瘤、滑膜肉瘤等),导致其发病率在统计上有...
2026-04-05
-
喉癌-声音嘶哑三个月当咽炎治,喉科医生让做喉镜发现了声带白斑
从“咽炎”到“声带白斑”:三个月的嘶哑与一次关键的喉镜 引言:被忽略的“小毛病” 李建国第一次觉得喉咙不对劲,是在去年开春。作为一名出租车司机,他总感觉嗓子眼里像卡了什么东西,吞咽时有异物感,起初以为是咽炎或上火,自行服用润喉片了事。类似的情况也发生在张大爷和尉大伯身上,他们都经历了长达数月的声音嘶哑,初期都误以为是感冒或普通喉炎,直到症状持续不退,才在家人...
2026-03-06
-
癌-过长几十年没管,反复糜烂最后确诊癌变
引言 在男性健康领域,一些看似寻常的生理状况,若经年累月地忽视,可能潜藏着巨大的健康风险。过长,便是这样一个普遍存在却又常被轻视的问题。许多男性,尤其是中老年群体,可能数十年都未对其加以关注和干预,殊不知,长期的过长状态,与一种相对罕见但后果严重的恶性肿瘤——癌之间,存在着千丝万缕的联系。临床上,不乏因过长、部位反复出现糜烂、溃疡而拖延就诊,最终被确诊为癌的...
2026-03-10
-
色素痣-黑色素细胞增生
色素痣,俗称“痣”或“黑痣”,几乎是每个人皮肤上都存在的“印记”。它们或大或小,或平或凸,颜色深浅不一,是皮肤最常见的良性肿瘤之一。尽管多数色素痣终身无害,但其形成机制、类型区分以及与恶性黑色素瘤的潜在关联,始终是公众关注和医学研究的重点。本文旨在系统阐述色素痣的本质——黑色素细胞的良性增生,深入剖析其成因、分类、临床特征、诊断方法及科学管理策略,以期为读者...
2026-04-18
-
软下疳-外阴溃疡疼痛,链杆菌阳性
摘要 软下疳是一种由杜克雷嗜血杆菌(Haemophilus ducreyi)引起的经典性传播疾病,临床上以生殖器部位出现一个或多个疼痛性溃疡,并常伴发腹股沟淋巴结肿大、化脓及破溃为典型特征^。其病原体为一种革兰染色阴性的短棒状链杆菌,显微镜下可见其呈鱼群状排列,此特征是实验室诊断的重要依据^。本文旨在系统阐述软下疳的病原学、临床表现、诊断与鉴别诊断,重点围绕...
2026-04-29
-
腿痛-腿痛走一会就要歇,血管外科医生说这是间歇性跛行
引言 在日常生活的行走中,你是否曾经历过这样的困扰:开始时步履轻松,但走了一段路后,小腿或臀部便传来阵阵酸痛、沉重,甚至麻木感,迫使你不得不停下脚步。稍作休息后,不适感神奇般消退,你又能继续前行,但不久后症状再次袭来,如此循环往复。这种“走走停停”的步态,在医学上被称为“间歇性跛行”。它并非简单的“人老腿先老”或“缺钙”,而常常是身体,特别是下肢血管系统发出...
2026-04-23
-
过敏性紫癜-孩子腿上起红点当过敏,儿科医生说这是血管炎要查尿
引言:被误解的“红点”——从皮肤到系统的警报 孩子活泼好动,腿上突然出现一片片红色斑点,不痛不痒,这场景在许多家庭中都曾上演。多数家长会将其归咎于蚊虫叮咬、湿疹或食物过敏,采取外用药膏或抗过敏药物处理。若这些红点具有几个关键特征: 集中分布于双小腿、脚踝及臀部,且呈对称性;颜色为鲜红或紫红,微微凸起于皮肤;最关键的是,用手指按压后颜色不消退 ,那么,这极有可...
2026-03-29
-
血管内皮生长因子- VEGF
血管内皮生长因子(VEGF):血管生成的“指挥家”与疾病治疗的关键靶点 一、VEGF的分子结构与家族图谱 血管内皮生长因子并非单一的蛋白质,而是一个功能多样、成员众多的蛋白家族。通常所称的VEGF,主要指的是该家族的核心成员——VEGF-A。该家族还包括VEGF-B、VEGF-C、VEGF-D、VEGF-E(病毒编码)以及胎盘生长因子(Placental G...
2026-04-09
-
角化棘皮瘤-半球形结节中央角栓,可自行消退
在皮肤肿瘤的谱系中,角化棘皮瘤以其独特且充满迷惑性的临床表现,成为皮肤科医生与病理学家关注的焦点。它通常以“不速之客”的姿态突然出现,表现为一个快速增长的半球形结节,中央常有一个标志性的角质栓,形似微小的火山口。最令人称奇的是,与多数肿瘤不同,角化棘皮瘤往往能在数月内自行消退,这一自限性过程为其蒙上了一层神秘色彩。因其在临床上与某些皮肤恶性肿瘤(尤其是鳞状细...
2026-05-07
-
致残性全硬化性硬斑病-儿童,关节挛缩
摘要 致残性全硬化性硬斑病是一种主要发生于儿童的特殊亚型局限性硬皮病,具有显著的侵袭性与致残风险。其核心危害之一在于病变深度累及真皮、皮下组织、筋膜、肌肉乃至骨骼,导致关节活动严重受限,最终形成屈曲挛缩畸形,对患儿的生长发育与生活质量造成深远影响。本文将从疾病概述、关节挛缩的病理机制、临床表现、诊断、综合治疗策略及家庭护理等方面进行系统性阐述。 一、 疾病概...
2026-04-07
-
结节性硬化-面部皮脂腺瘤,癫痫智力低下
结节性硬化症的临床三联征:皮脂腺瘤、癫痫与智力低下 结节性硬化症(Tuberous Sclerosis Complex, TSC)是一种常染色体显性遗传的神经皮肤综合征,其临床表现复杂多样,可累及皮肤、神经系统、肾脏、心脏、肺及眼等多个器官系统。在众多临床表现中, 面部皮脂腺瘤、癫痫发作和智能减退 构成了该疾病最具标志性的临床三联征,是临床识别与诊断TSC的...
2026-04-19
-
鞭虫病-慢性腹泻,大便鞭虫卵
本文旨在系统探讨由毛首鞭形线虫(鞭虫)感染引起的慢性腹泻的病因学、病理生理机制、临床表现、诊断方法及综合防治策略。文章首先概述鞭虫的生活史与感染途径,继而深入分析其导致肠道慢性炎症、黏膜损伤及功能紊乱的病理过程,详细阐述由此引发的慢性腹泻的临床特点与并发症。结合现有医学证据,提出诊断、治疗及预防的一体化方案,以期为临床实践和公共卫生干预提供参考。 一、 引言...
2026-03-27
-
衣原体肺炎-婴幼儿肺炎,沙眼衣原体
在婴幼儿肺炎的诸多病原体中,沙眼衣原体(Chlamydia trachomatis, CT)占据着独特且重要的地位。与典型细菌或病毒引起的急性肺炎不同,沙眼衣原体肺炎起病隐匿、病程迁延,症状常不典型,易被家长甚至初诊医生忽视,但其对婴幼儿呼吸系统的潜在影响不容小觑。该病主要通过母婴垂直传播,常见于1至3个月龄的婴儿,是6个月以下婴儿肺炎的重要病原之一,国内研...
2026-03-25
-
色素沉着息肉综合征-口唇黑斑肠息肉
在日常生活中,口唇周围出现黑斑常被误认为是普通的色素沉着或“胎记”。在某些情况下,这些看似不起眼的斑点,却可能是一种名为“色素沉着息肉综合征”(Peutz-Jeghers Syndrome, PJS)的罕见遗传性疾病发出的早期皮肤信号。这是一种以皮肤黏膜色素沉着和胃肠道多发息肉为特征的综合征,其背后隐藏着不容忽视的肠道健康风险乃至肿瘤易感性^。本文将深入解析...
2026-03-20
-
肝癌-手术切除了肝癌,五年没复发是不是就治愈了?肝胆外科医生
跨越五年里程碑:临床治愈与终身随访的辩证——一位肝胆外科医生的视角 引言:五年之期的希望与隐忧 “手术很成功,五年没复发,恭喜您!”在肝胆外科的诊室里,医生对复查结果良好的患者说出这句话时,总是带着由衷的喜悦。对于肝癌患者而言,术后五年无病生存是一个极具象征意义的胜利节点。大量临床数据表明,肝癌术后复发多集中在前三年,五年后复发概率会大幅下降。医学界普遍将“...
2026-03-09
-
结核性关节炎-慢性单关节炎,结核病史
摘要 结核性关节炎,作为一种由结核分枝杆菌引起的慢性、感染性单关节炎,在临床实践中因其起病隐匿、症状不典型而常被忽视或误诊。它通常继发于身体其他部位的结核病灶,是结核病全身播散的一种局部表现。本文旨在系统阐述结核性关节炎,特别是其作为慢性单关节炎的临床特征、诊断要点、鉴别诊断以及诊疗策略,以提高临床医生对此病的认识,减少误诊漏诊,改善患者预后。 一、 概述与...
2026-03-26
-
裂头蚴病-皮下包块,贴生蛙肉史
裂头蚴病是由曼氏迭宫绦虫的幼虫——裂头蚴寄生人体引起的一种人兽共患寄生虫病。其临床表现复杂多样,其中皮下裂头蚴病是最常见的临床类型之一,典型特征为出现游走性皮下结节或包块。大量流行病学调查与临床病例证实,这种皮下病变与一种特定的感染史——使用生蛙肉贴敷伤口或患处(即“贴生蛙肉史”)——存在极为密切的病因学联系。本文旨在系统阐述裂头蚴病皮下包块的临床表现、病理...
2026-04-28
-
肝转移癌-肠癌术后三年肝上发现占位,肝胆外科评估后二次手术切
引言:当转移的阴影再次降临 对于许多结直肠癌患者而言,成功完成初次根治性手术,意味着赢得了一场至关重要的战役。术后的康复之路并非总是一帆风顺。据统计,高达50%至70%的结直肠癌患者在术后会出现肝转移,其中一部分甚至在术后三年内,于定期复查中发现肝脏出现了新的“占位性病变”。这无疑是给患者和家庭投下的一片沉重阴影。当影像报告上出现“肝内多发占位,考虑转移瘤可...
2026-03-08
-
催乳素瘤- PRL升高,溴隐亭治疗有效
摘要 催乳素瘤是临床上最常见的功能性垂体腺瘤,其核心特征是垂体泌乳素细胞异常增生并分泌过量的催乳素(PRL),导致高催乳素血症及相关临床症状^。该疾病对患者,尤其是育龄期女性的生殖健康及生活质量构成显著影响^。以溴隐亭为代表的多巴胺受体激动剂是国内外公认的一线药物治疗方案,其在降低血清PRL水平、缩小肿瘤体积及改善临床症状方面具有明确的疗效^。本文旨在系统阐...
2026-03-06
-
胃癌-年轻女性贫血多年,胃镜发现皮革胃
被贫血掩盖的胃之“铠甲”:一例年轻女性皮革胃的深度启示 引言:当贫血成为“报警信号” 在临床实践中,年轻女性出现慢性贫血是一个常见但原因复杂的征象。它可能源于营养因素、月经过多、血液系统疾病,亦可能是一些隐匿性慢性失血或消耗性疾病的外在表现。其中,消化道肿瘤,尤其是胃癌,因其典型症状如腹痛、黑便、消瘦等更易被警惕,但对于一种特殊类型的胃癌——“皮革胃”而言,...
2026-05-01
-
麻风病-皮肤感觉障碍,外周神经粗大
麻风病,作为一种由麻风分枝杆菌引起的慢性传染病,其历史与人类文明交织,常被蒙上恐惧与误解的面纱。从现代医学视角审视,麻风病有其独特的病理轨迹与临床特征。其临床表现虽具多样性,但核心在于对皮肤与周围神经系统的选择性侵犯。其中, 皮肤感觉障碍 与 周围神经粗大 构成了麻风病最具特征性、也最常导致诊断与功能损害的两大核心症候群。理解这两种症状,不仅是识别这一“模仿...
2026-04-29
-
肝癌-乙肝携带者多年不复查,肚子胀发现肝癌破裂出血
引言:被忽视的“小毛病”与致命的转折 在快节奏的现代生活中,许多人都背负着健康“历史问题”前行,其中慢性乙型肝炎病毒(HBV)携带者是一个庞大的群体。对于部分携带者而言,由于早期可能没有明显症状,加之对疾病进展的轻视或对长期服药的顾虑,定期复查常常被置于次要位置,甚至被完全遗忘。肝脏是一个“沉默的器官”,当其内的隐患悄然滋长、最终爆发时,往往已酿成无法挽回的...
2026-03-18
-
胃癌-年轻女性贫血多年补铁无效,消化科医生让做胃镜发现了皮革
在临床工作中,消化科医生时常遇到一些“常规治疗无效”的病例,这些病例往往隐藏着更严重的健康威胁。年轻女性因贫血就诊是常见现象,通常与月经量过多、营养摄入不足等因素相关,口服铁剂补充治疗多能奏效。当贫血持续多年且对补铁治疗毫无反应时,这便不再是简单的营养性贫血,而可能是一个需要深究的危急信号。胃癌,尤其是被称为“皮革胃”的特殊类型,正可能以这种隐匿的方式悄然进...
2026-03-07
-
白血病-孩子低烧半个月,血常规正常,三个月后确诊白血病,血液
引言:一个“正常”结果带来的麻痹与挑战 在儿科门诊,发热是最常见的就诊原因之一。当伴随发热的孩子拿到一份看似“正常”的血常规报告时,家长和部分初诊医生往往会松一口气,倾向于诊断为普通病毒感染,并采取观察或常规对症治疗。临床中不乏这样的案例:孩子持续低烧半个月甚至更久,反复检查血常规均无显著异常,却在数月后被确诊为白血病。这种“血常规正常”的表象,如同一层迷雾...
2026-03-10
-
腰痛-腰痛腿麻当椎间盘突出,脊柱外科医生看了片子说椎管里长了
腰痛伴随腿麻,是骨科与脊柱外科门诊中最常见的症状组合之一。对于许多患者乃至部分非专科医生而言,这一症状组合的首选诊断往往是“腰椎间盘突出症”。确实,椎间盘退变、纤维环破裂导致髓核突出,压迫神经根或脊髓,是引起此类症状的最常见病理基础。典型的症状包括腰部疼痛,以及向下肢放射的疼痛、麻木或无力感,在咳嗽、打喷嚏或久坐时可能加重。影像学检查,尤其是磁共振成像(MR...
2026-03-27
-
蛲虫病-夜间瘙痒,透明胶纸法找虫卵
摘要 :蛲虫病是一种全球范围内广泛流行的肠道寄生虫病,尤其在儿童群体中感染率较高。其最显著且令人困扰的症状是夜间及会的剧烈瘙痒。本文旨在系统阐述蛲虫病的病原学特点、临床表现,并重点剖析其首选诊断方法——透明胶纸法的原理、操作流程、优势及在临床实践中的应用价值。文章也将概述该病的传播途径、治疗原则及综合预防策略,以期为公众认知和临床诊疗提供全面的参考。 一、 ...
2026-04-26
-
尿分叉-尿分叉当前列腺炎治了一年,泌尿外科医生说是尿道狭窄
尿分叉,是许多男性在排尿时可能遇到的现象。它可能是一过性的生理反应,也可能是某种泌尿系统疾病的信号。当这一症状长期存在,并伴随尿线变细、排尿费力、尿频尿急时,患者和医生常常首先将目光投向“前列腺炎”这一常见诊断。临床实践中存在这样一种情况:患者按照前列腺炎规范治疗数月甚至一年,症状却改善甚微,直至前往泌尿外科进行深入检查,才被明确诊断为“尿道狭窄”。这一年的...
2026-03-06
-
脑转移癌-乳腺癌术后五年突然头痛呕吐,神经外科会诊发现脑转移
五年平稳期后的颅内警报:一例乳腺癌术后脑转移的深度剖析 摘要 :本文通过一例乳腺癌根治术后五年,以突发头痛、呕吐为首发症状,最终确诊为脑转移瘤的典型病例,系统梳理了乳腺癌脑转移的常见临床症状谱、病理生理机制、现代影像学与分子诊断方法,并探讨了以神经外科为主导的多学科综合治疗策略。文章强调,对于有乳腺癌病史的患者,即使术后多年,任何新发的神经系统症状都需高度警...
2026-03-07
-
食管腺癌- Barrett食管不复查,十年后查出腺癌
Barrett食管,作为一种因长期胃食管反流导致食管下段鳞状上皮被柱状上皮替代的病理状态,已被公认为食管腺癌最重要的癌前病变。其本身或许不产生特异症状,却像一枚埋藏在食管黏膜下的“定时”,其潜在的风险在于缓慢而隐匿的癌变进程。临床上,医生总会向确诊患者强调定期内镜复查的重要性。设想这样一位患者:他在十年前被明确诊断为Barrett食管,或许因症状轻微、心存侥...
2026-04-22
-
血小板减少-牙龈出血止不住,血液科医生说血小板只有一万
引言:从一次“止不住”的牙龈出血说起 在日常生活中,牙龈出血是许多人都会遇到的“小问题”,常常被归咎于“上火”、刷牙太用力或缺乏维生素C。当一位患者因牙龈持续渗血、难以止住而前往医院,最终在血液科得到“血小板计数只有一万”的诊断时,这便不再是寻常的口腔问题,而是一声来自身体深处的、关乎生命健康的紧急警报。血小板,这个在常规体检血常规单上看似不起眼的指标,当其...
2026-03-28
-
室管膜瘤-第四脑室占位,梗阻性脑积水
在神经外科与神经肿瘤学领域,第四脑室区域的占位性病变始终是临床关注的重点与难点。该区域位于小脑与脑干之间,是脑脊液循环通路的关键枢纽,解剖结构复杂且功能至关重要。其中,起源于脑室系统室管膜细胞的 室管膜瘤 是此区域最常见的原发性肿瘤之一^。此类肿瘤的生长不仅因其占位效应直接压迫毗邻的脑干、小脑等重要神经结构,更常因阻塞脑脊液循环通路而引发 梗阻性脑积水 ,导...
2026-03-06
-
胸膜间皮瘤-石棉接触史胸水查不出原因,胸外科胸腔镜活检确诊
在呼吸科或胸外科门诊,我们有时会遇到这样一类患者:他们多为中老年男性,有明确的石棉接触史(可能是在数十年前的建筑、造船或矿业工作中),因逐渐加重的胸闷、气促和持续性胸痛前来就诊。胸部影像学检查,如X光或CT,往往提示存在中到大量的胸腔积液,即通常所说的“胸水”^。反复的胸腔穿刺抽液进行常规生化、细胞学检查,却常常回报为“未见恶性肿瘤细胞”或“渗出液,原因待查...
2026-03-07
-
肝癌-肝癌术后五年没复发,患者问是不是根治了,医生没有直接回
引言:五年之期,希望与困惑并存 在肝癌的治疗征程中,“五年”是一个被赋予了特殊意义的时间标尺。对于经历了手术洗礼的患者而言,能够平安度过术后五年且无复发迹象,无疑是一个值得庆祝的里程碑。 它通常被视为临床治愈的重要参考标准,意味着患者体内的肿瘤负荷已被成功清除或得到长期有效控制,长期生存的概率显著提高。 当患者满怀期待地向医生求证“是否根治”时,得到的回答往...
2026-03-08
-
膀胱癌-尿血以为是尿路感染,吃了抗生素还出血,膀胱镜检查发现
五十多岁的陈先生(化名)在一个多月前发现自己小便颜色变红,像洗肉水一样,但身体没有任何疼痛或不适。 他首先想到的是常见的尿路感染或“上火”,于是自行去药店购买了抗生素服用。服药一周后,血尿症状并未如预期般消失,时有时无,这让他心里开始打鼓。 在家人催促下,他最终前往医院就诊。这个案例并非个例,临床上,约80%-90%的膀胱癌患者首发的、最典型的症状正是这种 ...
2026-03-07
-
肿瘤标志物-筛查,随访
在癌症防控与管理的全链条中,早期发现与有效监测是改善预后的两大基石。肿瘤标志物检测,通过分析血液、体液等样本中由肿瘤细胞产生或机体应对肿瘤而异常改变的物质,为此提供了重要的辅助手段^。其在临床实践中主要扮演两大核心角色:一是作为面向特定高危人群的早期筛查“哨兵”,力图在症状出现前捕捉风险信号;二是作为已确诊患者的随访“导航仪”,用于评估疗效、预警复发及判断预...
2026-04-07
-
骨转移癌-肺癌骨转移腿疼走不了路,骨科医生说可以做个手术止痛
引言:无法行走之痛背后的生命困境 “医生,我的腿疼得一步都走不了了。”——在肿瘤科或骨科门诊,这声来自肺癌骨转移患者的痛苦倾诉,已不再罕见。随着肺癌诊疗水平的提升,患者生存期得以延长,但肿瘤细胞向骨骼的“迁徙”与破坏,却成为影响晚期患者生活质量的最严峻挑战之一。骨骼,这具支撑我们躯体、赋予我们行动自由的坚硬框架,一旦被转移癌细胞侵蚀,便会引发剧烈疼痛、病理性...
2026-03-27
-
骨嗜酸性肉芽肿-骨溶骨性破坏,良性
骨嗜酸性肉芽肿——一种表现为溶骨性破坏的良性骨病探究 骨嗜酸性肉芽肿是一种以骨骼系统局限性溶骨性破坏为特征的良性病变,本质为朗格汉斯细胞的克隆性增生。本文系统阐述了该病的流行病学特征、病因假说、病理基础、临床表现与影像学特点,重点分析了其“良性溶骨性破坏”的独特性质,并综述了当前的诊断标准、鉴别诊断要点、个体化治疗策略及总体良好的预后,旨在深化临床及公众对这...
2026-03-29
-
腹水-腹水查不出原因,消化科医生让抽了腹水送病理找到癌细胞
腹水,即腹腔内异常积聚的液体,是多种疾病状态下常见的临床表现。当患者出现腹水,尤其是常规检查难以明确病因时,临床医生便面临着一项诊断挑战。消化科医生在面对“查不出原因”的腹水时,决定抽取腹水送病理学检查以寻找癌细胞,是一条关键且具有转折意义的诊断路径。这一决策不仅可能揭开腹水形成的隐匿面纱,更可能直接指向恶性肿瘤腹腔转移这一严重状况,从而彻底改变疾病的诊断分...
2026-04-14
-
黄体生成素- LH
生命周期的精准节拍器:深入解读黄体生成素(LH) 引言:下丘脑-垂体-性腺轴上的关键信使 在人体精密而复杂的内分泌网络中,下丘脑-垂体-性腺轴(HPG轴)是调控生殖与性发育的核心指挥系统。黄体生成素,作为该轴线上由腺垂体分泌的一种糖蛋白激素,扮演着不可或缺的信使与执行者角色。它并非孤立存在,而是与促卵泡生成素协同作用,共同精细调控着从青春期启动、月经周期运转...
2026-04-18
-
食管癌-吞咽梗阻感半年,胃镜发现食管全周狭窄
引言 食管癌是我国高发的消化道恶性肿瘤之一,其典型临床症状常表现为进行性吞咽困难、异物感及胸骨后疼痛。当患者出现长达半年的吞咽梗阻感,并通过胃镜检查发现食管全周性狭窄时,这通常提示病变已进入中晚期阶段,临床处理面临严峻挑战。全周性狭窄意味着肿瘤已沿食管壁环形浸润生长,严重阻碍食团通过,并显著影响患者的生活质量与营养状况。本文旨在系统阐述此类病例的病理机制、诊...
2026-03-07
-
血栓素-血小板聚集
摘要 :血栓形成是心血管疾病的主要病理基础,而血小板聚集是血栓形成的核心环节。血栓素A2(TXA2)作为花生四烯酸代谢的关键产物,是体内最强的血小板聚集促进剂和血管收缩剂之一。本文系统阐述了血栓素在血小板聚集过程中的分子机制,包括其生物合成途径、信号转导通路以及对血小板活化、黏附、聚集和释放反应的调控作用。文章梳理了基于血栓素通路的关键抗血小板药物(如阿司匹...
2026-03-22
-
转化生长因子- TGF
作者: 百度文心助手 日期: 2026年03月07日 关键词: 转化生长因子-β (TGF-β);信号转导;细胞周期;发育;免疫调节;纤维化;癌症 引言:从神秘因子到调控核心 在生命科学的宏大乐章中,存在着少数几种分子,它们如同交响乐团的指挥,协调着细胞增殖、分化、迁移、凋亡等一系列复杂而精密的生命活动。转化生长因子-β (Transforming Grow...
2026-04-09
-
脂肪肝-重度脂肪肝患者坚持跑步一年,复查时医生问是不是吃了什
一、引言:一个出乎意料的复查场景 在许多人的认知里,疾病的逆转,尤其是像重度脂肪肝这样的代谢性疾病,总离不开药瓶和处方。当王明(化名)这位曾经的“重度脂肪肝”患者,时隔一年再次走进消化科诊室时,一场由一张超声报告单引发的对话,却颠覆了这种常规的想象。 “王先生,你的肝脏B超显示……脂肪浸润程度从重度转为轻度了。最近是不是吃了什么特效药,或者用了什么新的治疗方...
2026-03-07
-
腺病毒感染-咽结膜热,游泳池传播
引言 在炎炎夏日,公共游泳池是大众消暑纳凉、锻炼身体的热门场所。这片碧波荡漾的水域在带来清凉与欢乐的也可能成为某些病原体传播的温床,其中,腺病毒及其引发的咽结膜热尤为值得关注。这种以发热、咽炎和急性结膜炎为典型三联征的急性上呼吸道感染,因其与游泳池环境的特殊关联,常被称为“泳池热”。本文将深入剖析腺病毒,特别是其导致咽结膜热的病原学特征、在游泳池环境中的传播...
2026-04-06
-
非精原细胞瘤-胚胎癌成分,化疗后肿瘤标志物下降
化疗应答的生化信号:非精原细胞瘤-胚胎癌成分患者肿瘤标志物下降的解读与临床启示 引言:肿瘤标志物在生殖细胞肿瘤管理中的基石作用 非精原细胞瘤(Non-Seminomatous Germ Cell Tumors, NSGCTs)是男性生殖细胞肿瘤中高度异质性的一类,其中胚胎癌(Embryonal Carcinoma)成分以其侵袭性强、增殖快速和转移风险高的特点...
2026-04-10
-
高香草酸- HVA
高香草酸,化学名称为4-羟基-3-甲氧基,其分子式为C₉H₁₀O₄,分子量约为182.17。 在物理性状上,它通常呈现为白色至浅棕色或灰白色的结晶粉末,熔点约为142-145°C。 作为一种酚类化合物,高香草酸具备一定的荧光特性,尤其是在酸性条件下可与铁离子发生氧化还原反应,生成具有更长荧光寿命的二聚体,这一特性也被应用于其检测分析中。 从生物化学角度看,高...
2026-03-21
-
癌-血糖突然升高伴消瘦,内分泌科医生让查
在临床诊疗中,内分泌科医生时常会遇到一类特殊的患者:他们既往没有糖尿病史,却在短期内出现难以解释的血糖显著升高,同时伴有进行性的、无明显原因的体重下降。当常规的降糖治疗效果不佳,或血糖波动难以用普通2型糖尿病解释时,经验丰富的医生往往会将目光投向腹腔深处的一个重要器官——,并建议进行针对性检查以排除癌的可能。这种关联并非偶然,而是源于独特的生理结构和癌对内分...
2026-03-11
-
钙质沉着-皮下钙化
在临床影像学检查或皮肤科门诊中,“皮下钙化灶”或“钙质沉着”是一个常被提及的发现。它指代的是钙盐(主要为磷酸钙和碳酸钙)在皮肤及其下方软组织中的异常沉积,形成肉眼不可见但可通过影像或触诊感知的致密硬结或斑块。这一现象既可能是既往组织损伤愈合后遗留的“疤痕”印记,也可能是体内代谢失衡发出的警示信号。因其成因复杂、表现多样,且多数情况下虽为良性,却仍需与恶性病变...
2026-03-20
-
视黄醇结合蛋白4-胰岛素抵抗
视黄醇结合蛋白4(Retinol-Binding Protein 4, RBP4)长期以来被认为是负责在血液中特异性转运维生素A(全反式视黄醇)的主要载体蛋白,对于维持视觉、免疫及上皮组织健康至关重要。自21世纪初以来,一系列突破性研究揭示了RBP4的另一重关键身份:一种由脂肪组织分泌的脂肪因子,其在肥胖、2型糖尿病、代谢综合征等疾病的胰岛素抵抗发生发展中扮...
2026-03-19
-
肾嫌色细胞癌-体检发现肾占位,手术预后良好
在肾脏恶性肿瘤的谱系中,肾嫌色细胞癌以其相对惰性的生物学行为和良好的预后,常被医学界称为“幸运癌”。随着健康体检的普及,越来越多的肾脏占位性病变在无症状阶段被偶然发现,其中就包括肾嫌色细胞癌。这种肿瘤通常生长缓慢,早期缺乏典型症状,使得定期体检成为早期诊断的关键窗口。本文旨在全面梳理肾嫌色细胞癌的临床病理特征、诊断思路、治疗策略及长期预后,为公众和患者提供科...
2026-03-08
-
黄色瘤-黄褐色斑块,血脂异常
引言:来自皮肤的无声警报 在日常生活中,我们偶尔会在自己或他人的眼睑、关节等处发现一些不痛不痒的黄色或黄褐色斑块、丘疹。这些看似微不足道的皮肤改变,医学上称为“黄色瘤”。它们并非简单的皮肤瑕疵或衰老标记,而常常是体内脂质代谢紊乱、血脂异常在皮肤上的直观投影。这些“脂质信使”的出现,可能正悄然揭示着血管健康所面临的潜在危机。理解黄色瘤的本质,不仅关乎皮肤美观,...
2026-04-18
-
甲状腺髓样癌-甲状腺结节伴腹泻,降钙素明显升高
在常规体检或门诊中,甲状腺结节与腹泻常被视作独立的健康问题分别处理。甲状腺结节多数为良性,仅需定期观察;腹泻则常归因于感染、饮食不当或肠易激综合征等。当这两种情况在同一个体身上并存,特别是当实验室检查揭示出血清降钙素水平异常显著升高时,临床医生需保持高度警惕。这一组合可能是甲状腺髓样癌发出的重要信号。甲状腺髓样癌虽然仅占所有甲状腺癌的约5%-10%,但其具有...
2026-03-12
-
胼胝-足底弥漫性角化,摩擦引起
引言 在我们的日常生活中,足底皮肤变硬、增厚形成俗称的“老茧”,是一种极为普遍的现象。这种看似微不足道的皮肤变化,实则是人体应对长期机械刺激的一种复杂而精妙的保护性反应。当这种角质增厚超出正常生理范畴,或与特定病理状态相结合时,便会演变为困扰人们行走、影响生活质量的足部问题。其中,由长期摩擦压迫引起的胼胝(callus)与具有遗传背景的弥漫性掌跖角化病(di...
2026-03-31
-
鲍温病-红色斑块,鳞状细胞癌原位
警惕皮肤上的“伪装者”:鲍温病——一种特殊的皮肤原位鳞状细胞癌深度解析 摘要 鲍温病是一种独特且具有潜在风险的皮肤疾病,医学上被定义为皮肤原位鳞状细胞癌。它代表着皮肤恶性肿瘤的一个早期阶段,其癌细胞尚“规规矩矩”地局限在皮肤最表层的表皮内,尚未突破基底膜向下方的真皮层发生侵袭性生长。由于其临床表现常与慢性湿疹、皮炎或银屑病等良性皮肤病相似,极易被患者甚至非专...
2026-04-29
-
裂谷热-发热肝炎出血,接触牛羊
裂谷热:发热、肝炎、出血背后的牛羊接触风险与防控策略 摘要 裂谷热(Rift Valley fever, RVF)是一种由裂谷热病毒(RVFV)引起的人畜共患急性传染病。该病最初在动物间流行,可导致以牛、羊为代表的反刍动物出现高流产率和幼畜高死亡率,同时也可感染人类,引发从自限性发热性疾病到重症肝炎、出血热及脑膜脑炎等一系列临床表现,其中出血性重症的病死率可...
2026-05-07
-
胃癌-胃癌全胃切除后,患者问怎么吃饭,医生说小肠会代偿
引言:告别胃囊,开启新的消化旅程 胃癌全胃切除术是治疗胃癌的重要外科手段,它意味着患者将与重要的消化器官——胃永久告别。这一改变无疑会引发患者及家属对“今后如何吃饭”、“营养如何吸收”、“身体能否承受”等一系列问题的深切焦虑与困惑。现代医学研究与临床实践表明,人体拥有令人惊叹的适应与代偿能力,尤其是小肠,将在术后扮演全新的核心角色。本文旨在系统阐述全胃切除术...
2026-03-28
-
胃淋巴瘤-胃部不适CT发现胃壁增厚,胃镜活检淋巴瘤
引言:胃壁增厚的影像学迷雾 在腹部增强CT检查中,胃壁的正常厚度通常不超过5毫米。当放射科医生在报告中写下“胃壁增厚”时,这个看似简单的描述,实际上打开了一扇通往复杂鉴别诊断的大门。胃壁增厚本身并非一种疾病,而是一个影像学征象,它像一道待解的谜题,其答案可能指向多种病理状态。常见的原因包括良性的慢性胃炎、胃溃疡,以及恶性的胃癌、胃间质瘤,也包括本文讨论的核心...
2026-04-10
-
胶质瘤-癫痫发作,MRI发现额叶占位
癫痫发作是神经科常见的急症与慢性病症,其背后病因复杂多样。在继发性癫痫的诸多病因中,颅内肿瘤,尤其是脑胶质瘤,占据着重要地位。胶质瘤作为中枢神经系统最常见的原发性肿瘤,其与癫痫发作的关联早已被临床广泛认知。当患者以癫痫为首发或主要症状就诊,并通过磁共振成像(MRI)发现额叶存在占位性病变时,临床思维的链条便自然地指向了胶质瘤的可能性。本文旨在系统阐述胶质瘤相...
2026-04-25
-
脑源性神经营养因子- BDNF
大脑的守护者:脑源性神经营养因子(BDNF)的生理功能、病理意义与未来潜能 引言 在探索大脑奥秘的漫长旅程中,科学家们发现了一种对神经系统的发育、维持与修复至关重要的蛋白质——脑源性神经营养因子(Brain-derived neurotrophic factor, BDNF)。自1982年首次从猪脑中被分离鉴定以来,BDNF因其广泛而强大的生物学功能,被誉为...
2026-04-09
-
肺吸虫病-咳嗽胸痛咳果酱样痰,生食石蟹
在众多食源性寄生虫病中,肺吸虫病是一种具有鲜明临床特征和明确感染途径的疾病。它并非通过空气或直接接触传播,而是与特定的饮食习惯紧密相连,尤其与某些地区食用淡水甲壳类动物的方式密切相关。当人们享受溪边捕捉石蟹的乐趣,或品尝未经充分烹制的“醉蟹”、“腌蟹”时,一种名为并殖吸虫的寄生虫可能随之潜入人体,最终在肺部“安家落户”,引发一系列以呼吸系统为主的症状。理解其...
2026-05-06