在神经外科与神经肿瘤学领域,第四脑室区域的占位性病变始终是临床关注的重点与难点。该区域位于小脑与脑干之间,是脑脊液循环通路的关键枢纽,解剖结构复杂且功能至关重要。其中,起源于脑室系统室管膜细胞的室管膜瘤是此区域最常见的原发性肿瘤之一^。此类肿瘤的生长不仅因其占位效应直接压迫毗邻的脑干、小脑等重要神经结构,更常因阻塞脑脊液循环通路而引发梗阻性脑积水,导致一系列危及生命的颅内压增高症状^。理解室管膜瘤的生物学特性、其导致第四脑室占位的机制,以及由此继发的梗阻性脑积水的病理生理过程,对于早期诊断、精准治疗和改善患者预后具有决定性意义^。
第一部分:室管膜瘤——第四脑室最常见的占位性病变
室管膜瘤是一种起源于脑室系统与脊髓中央管内衬的室管膜细胞的神经上皮性肿瘤,约占所有颅内肿瘤的3%-5%^。其发病年龄呈现双峰分布,第一个高峰在儿童期(尤其是5岁左右),第二个高峰则在中年期(约35岁左右)^。在解剖分布上,幕下(颅后窝)室管膜瘤约占60%,其中绝大多数位于第四脑室;幕上(大脑半球)室管膜瘤约占40%^。
1.1 病理与生长特点
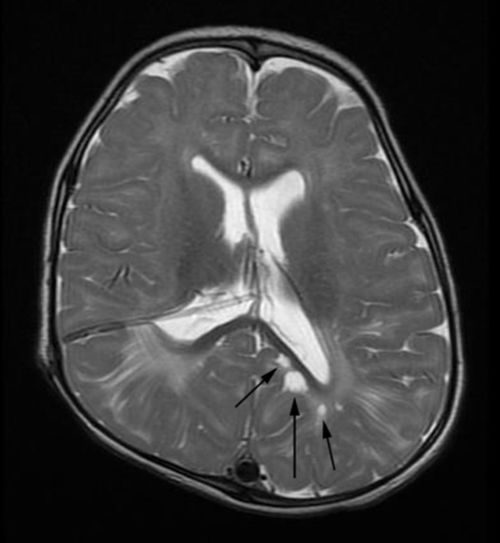
室管膜瘤在组织学上通常被世界卫生组织(WHO)中枢神经系统肿瘤分类定义为Ⅱ级,但存在间变性室管膜瘤(WHO Ⅲ级)等更具侵袭性的亚型^。典型的第四脑室室管膜瘤常起源于第四脑室的顶壁(后髓帆)或底壁(延髓背侧)^。其生长方式颇具特征性:肿瘤在第四脑室腔内呈“铸型生长”,即其形态与第四脑室的解剖空间高度契合,常常完全填充脑室腔^。更为关键的是,肿瘤组织可通过第四脑室的正常出口——正中孔(Magendie孔)和外侧孔(Luschka孔)向外生长,延伸至小脑延髓池,甚至向下经枕骨大孔突入上颈段椎管内,呈“舌状”覆盖于延髓和上颈髓的背侧^。这种生长模式不仅是导致临床症状多样化的原因,也极大地增加了手术全切除的难度和风险。
1.2 临床表现
第四脑室室管膜瘤的临床症状主要源于两方面:一是肿瘤的局部占位效应,二是其引发的梗阻性脑积水。
占位效应相关症状:肿瘤直接压迫或浸润脑干(尤其是延髓)和小脑,可导致一系列局灶性神经功能障碍。常见表现包括:因脑干网状结构受累所致的头痛(多为枕部或额部持续性钝痛)、恶心、呕吐(常为喷射性);因小脑及其传导通路受损引起的共济失调(表现为步态不稳、行走如醉酒状、指鼻试验不准)、眼球震颤;以及因延髓后组颅神经核团受压导致的吞咽困难、声音嘶哑、呛咳等^。部分患者可能出现强迫头位(头部倾斜以缓解症状)或颈项强直,这往往是肿瘤已延伸至枕骨大孔以下、刺激上颈髓神经根的征象,提示病情危重^。
梗阻性脑积水相关症状:这是更常见且可能迅速危及生命的症候群,将在下文详细阐述。
第二部分:从占位到梗阻——脑积水形成的病理生理机制
梗阻性脑积水是指由于脑脊液循环通路在脑室系统内的任何部位发生阻塞,导致脑脊液产生与吸收失衡,脑室内压力增高、脑室系统扩张的一种病理状态^。第四脑室室管膜瘤是引起梗阻性脑积水的经典和常见原因之一^。
2.1 脑脊液循环与梗阻点
脑脊液主要由侧脑室脉络丛产生,流经室间孔进入第三脑室,再通过狭长的中脑导水管进入第四脑室。脑脊液通过第四脑室的正中孔和外侧孔流出,进入蛛网膜下腔,最终被蛛网膜颗粒吸收回静脉系统^。第四脑室恰似脑脊液流出脑室系统的“总阀门”。
2.2 室管膜瘤导致梗阻的机制
室管膜瘤主要通过以下两种主要方式阻塞这一关键通路:
1. 直接机械性阻塞:这是最主要的原因。肿瘤在第四脑室内生长,直接堵塞了中脑导水管的出口、第四脑室腔本身、或者正中孔和外侧孔,阻断了脑脊液从第三脑室向蛛网膜下腔的流动^。当中脑导水管或第四脑室出口被完全或部分堵塞时,上游的侧脑室和第三脑室便会因脑脊液积聚而进行性扩张,形成典型的梗阻性脑积水^。
2. 间接影响与分泌亢进:少数情况下,分泌活跃的脉络丛状瘤(亦可见于第四脑室)可通过过度产生脑脊液,超出吸收系统的能力而导致脑积水^。虽然典型的室管膜瘤并非以分泌功能为主,但肿瘤占位引起的局部炎症反应、出血或坏死物质释放,可能进一步加重蛛网膜下腔的粘连,影响脑脊液的吸收,从而与梗阻因素共同作用,加剧脑积水^。
2.3 病理生理后果
梗阻发生后,脑室内压力(颅内压)持续升高。持续的颅内高压不仅引发剧烈头痛、呕吐、视水肿等典型症状,更会导致两种严重的继发性损害:脑室周围白质水肿和弥漫性脑水肿^。脑室周围水肿是由于脑室内高压迫使脑脊液穿过室管膜进入周围脑组织所致;而弥漫性脑水肿则是颅内高压导致脑血流灌注减少、血脑屏障破坏、细胞代谢障碍的综合结果^。若不及时干预,进行性的脑疝(如小脑扁桃体下疝)可压迫延髓生命中枢,导致呼吸心跳骤停而死亡^。
第三部分:诊断与评估——影像学的关键角色
对于疑似第四脑室占位合并脑积水的患者,神经影像学检查是诊断和评估的金标准。
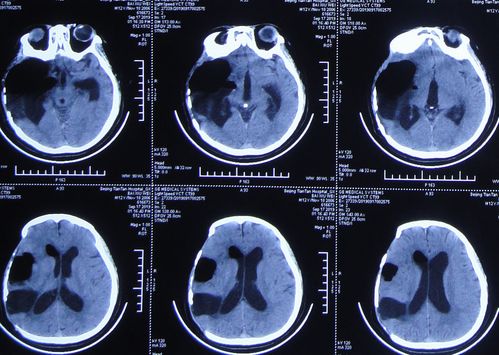
计算机断层扫描(CT):可快速显示脑室系统(尤其是侧脑室和第三脑室)的对称性扩张,提示梗阻性脑积水。CT也能较好地显示肿瘤内的钙化(室管膜瘤常见点状或斑片状钙化)以及急性出血^。
磁共振成像(MRI):是首选的检查方法,能提供多序列、多平面的高分辨率图像,福东健康网对肿瘤定位、定性及评估与周围重要结构的关系至关重要^。
平扫:室管膜瘤在T1加权像上常呈等或稍低信号,T2加权像上呈高信号。肿瘤常表现为边界相对清楚的分叶状肿块,内部信号常不均匀,反映其囊变、坏死、钙化或出血等成分^。
增强扫描:肿瘤实性部分通常呈现不均匀的明显强化,强化模式可为斑片状、结节状或环状^。典型的“铸型生长”模式在MRI矢状位和轴位图像上显示得尤为清晰,可见肿瘤填充第四脑室并可能经正中孔向下延伸^。
脑脊液电影成像:可用于动态评估脑脊液流动情况,直观显示在第四脑室出口等关键部位的梗阻^。
通过影像学,医生不仅能明确第四脑室占位的性质和范围,还能精确判断梗阻性脑积水的程度、脑室扩张的模式以及是否存在脑疝等紧急情况,为制定治疗方案提供决定性依据^。
第四部分:综合治疗策略——解除占位与分流积水
第四脑室室管膜瘤合并梗阻性脑积水的治疗是一个多步骤、综合性的过程,核心目标在于:解除脑脊液循环梗阻、降低颅内压、最大程度安全地切除肿瘤^。
4.1 术前处理与脑积水管理
对于因急性梗阻性脑积水导致严重颅内高压、有脑疝风险或意识障碍的患者,首要任务是紧急降低颅内压。传统上,可进行脑室外引流术(EVD),将导管置入侧脑室,将积聚的脑脊液引流至体外,快速缓解症状,为后续肿瘤切除手术创造条件^。外引流存在感染、出血等风险,且需严格管理。另一种更持久的术前处理方式是先行脑室-腹腔分流术(VP Shunt),建立永久性的脑脊液内引流通道。但分流术的缺点在于可能因压力调节不当引发过度引流(导致低颅压、硬膜下血肿),且存在肿瘤细胞通过分流管发生中枢神经系统外种植转移的潜在风险(尽管发生率低)^。选择术前分流还是术中一期解决脑积水,需根据患者具体情况(如年龄、症状严重程度、肿瘤可切除性评估)权衡利弊。
4.2 肿瘤切除术——根本性治疗
手术切除是治疗室管膜瘤、从根本上解除梗阻的基石。手术通常采用后颅窝正中入路,目标是在保护脑干、颅神经和重要血管的前提下,实现肿瘤的最大安全范围切除(Gross Total Resection, GTR)^。由于肿瘤常与第四脑室底(即脑干背侧)粘连紧密,全切手术极具挑战性,对术者的显微外科技术要求极高^。术中神经电生理监测(如脑干听觉诱发电位、体感诱发电位、运动诱发电位等)是保障手术安全、减少神经功能损伤的重要辅助手段^。对于未能全切的肿瘤,术后残留是复发的主要根源。
4.3 术后辅助治疗与长期管理
放射治疗:对于未能全切的Ⅱ级室管膜瘤、所有间变性(Ⅲ级)室管膜瘤,或复发风险高的患者,术后辅助放疗是标准治疗。目前多采用适形调强放疗(IMRT) 或质子治疗,精准照射肿瘤床及可能的亚临床病灶,以控制局部复发^。
化疗:在儿童患者、年轻成人或复发/难治性病例中,化疗的作用日益受到重视。常用的化疗方案包括基于铂类、依托泊苷、环磷酰胺等药物的组合^。
脑积水处理:肿瘤成功全切除后,脑脊液通路通常得以再通,脑积水可能自行缓解。若术后脑积水持续存在或复发,则需考虑行第三脑室底造瘘术(ETV) 或脑室-腹腔分流术(VP Shunt)^。ETV通过在第三脑室底部制造一个瘘口,使脑脊液绕过梗阻部位(如中脑导水管或第四脑室)直接流入脚间池,是一种生理性分流,避免了植入分流装置及其相关并发症^。
康复与随访:术后患者常需进行神经功能康复训练,以改善共济失调、吞咽困难等症状。长期定期随访(包括临床评估和头颅MRI复查)至关重要,旨在早期发现肿瘤复发或进展,以及监测分流管功能(若已安置)^。
结论与展望
第四脑室室管膜瘤作为一种兼具局部侵袭性和脑脊液通路阻塞双重危害的肿瘤,其临床管理是一项系统工程。从病理生理上看,肿瘤的“铸型生长”特性使其极易堵塞第四脑室这一脑脊液循环的“咽喉要道”,从而引发危及生命的梗阻性脑积水^。在诊断上,高分辨率MRI是揭示肿瘤特征、明确梗阻部位和评估脑积水严重程度的基石^。治疗上,应以神经外科手术为核心,力求在保护神经功能的前提下最大程度切除肿瘤,从根本上解除梗阻;根据病情需要,灵活运用脑室外引流、分流术或第三脑室造瘘术来管理脑积水;术后辅以放疗和/或化疗以巩固疗效、降低复发风险^。
未来的研究方向包括:利用分子病理学对室管膜瘤进行更精确的分型(如RELA融合基因阳性型),以指导个体化治疗和预后判断;发展更先进的术中成像和导航技术,以提高肿瘤切除的精确性和安全性;以及探索针对特定分子靶点的新型药物和免疫疗法,为复发或难治性患者提供更多选择。通过对这一疾病链——从室管膜瘤、第四脑室占位到梗阻性脑积水——的深入理解和多学科综合诊疗,有望持续改善患者的生存质量与长期预后。
