五年平稳期后的颅内警报:一例乳腺癌术后脑转移的深度剖析
摘要:本文通过一例乳腺癌根治术后五年,以突发头痛、呕吐为首发症状,最终确诊为脑转移瘤的典型病例,系统梳理了乳腺癌脑转移的常见临床症状谱、病理生理机制、现代影像学与分子诊断方法,并探讨了以神经外科为主导的多学科综合治疗策略。文章强调,对于有乳腺癌病史的患者,即使术后多年,任何新发的神经系统症状都需高度警惕脑转移可能,早期诊断与精准干预是改善预后的关键。
引言:从“治愈”到复发转移的临床挑战
乳腺癌是全球女性最常见的恶性肿瘤之一,随着诊疗技术的进步,患者生存期显著延长。根治性手术并非终点,术后复发转移,尤其是远处转移,仍是影响长期生存的主要威胁。大脑作为血供丰富的器官,是乳腺癌常见的远处转移部位之一,发生率约为10%-15%,在三阴性或HER2阳性亚型中风险更高,可达30%-50%。脑转移不仅严重影响患者的生活质量,其诊断与治疗也极具挑战性。本文所述案例——术后五年平稳期突然出现神经系统症状,正是临床中需要高度警惕的典型情景。
一、 症状解码:头痛呕吐背后的病理生理学
患者以“突发头痛、呕吐”为主要表现,这并非偶然。头痛是乳腺癌脑转移最常见和最早期的症状之一,发生率极高。其典型特征为持续性、进行性加重的钝痛或胀痛,常在清晨起床时或躺下后加重,咳嗽、用力或改变体位亦可诱发或加剧。这种头痛与普通紧张性头痛或偏头痛不同,常规止痛药物往往效果不佳或无效。其根本原因在于颅内占位性病变(转移瘤)及其引发的脑水肿,导致颅内压增高。颅腔是一个几乎封闭的骨性空间,当肿瘤生长或周围水肿带扩大时,颅内压力随之升高,牵拉、挤压或刺激了富含痛觉感受器的硬脑膜、血管壁,从而产生剧烈头痛。
呕吐,特别是突发性、喷射性的呕吐,常与剧烈头痛相伴发生,是颅内压增高的另一个典型标志。这种呕吐多与进食无关,呕吐前可有恶心,也可能毫无预兆地突然发生。其机制是颅内压急剧升高,直接刺激或压迫位于延髓的呕吐中枢所致。呕吐后,颅内压可能得到暂时性缓解,头痛稍有减轻,但会反复发作。若将此类症状简单归咎于“肠胃炎”而延误诊治,后果可能非常严重。
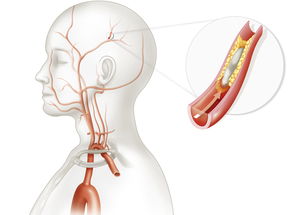
除了上述核心症状,乳腺癌脑转移还可表现为一系列局灶性神经功能缺损或刺激性症状,其具体表现取决于转移灶在大脑中的精确位置:
运动与感觉障碍:肿瘤压迫大脑皮层运动区或感觉区,可导致对侧肢体无力、麻木、偏瘫,或出现感觉异常(如针刺感、过电感)。患者可能突然出现拿不稳杯子、走路跛行或肢体不听使唤的情况。
癫痫发作:肿瘤刺激大脑皮层神经元异常放电,可引起癫痫,表现为肢体局部或全身抽搐、意识丧失、口吐白沫等。对于无癫痫病史的成年患者,新发癫痫需首要排除脑内结构性病变。
视觉与平衡功能异常:枕叶或视通路受压可导致视力下降、视野缺损(如一侧看不见)、视物重影(复视)。小脑或前庭系统受累则表现为共济失调、走路不稳、眩晕,如同醉酒状态。
认知与精神行为改变:额叶、颞叶等高级认知功能区受累,可能导致记忆力显著减退、注意力难以集中、计算或判断力下降、性格改变、情绪异常(如淡漠、抑郁、易怒)甚至出现幻觉、妄想等精神症状。这些改变常被患者及家属误认为“年纪大了”或“心情不好”,从而被忽略。
本案例中,患者术后五年突发头痛呕吐,强烈提示颅内压急性增高,是脑转移瘤引起占位效应和脑水肿的明确信号,必须立即进行神经影像学评估。
二、 精准诊断:神经外科会诊与现代影像技术
当乳腺癌患者出现可疑神经系统症状时,神经外科会诊是启动精准诊断流程的关键一步。会诊医生通过详细的神经系统体格检查,初步定位可能的病变区域。确诊必须依靠先进的影像学检查。
头颅磁共振成像(MRI):这是诊断脑转移瘤的首选和金标准影像学方法。与CT相比,MRI具有更高的软组织分辨率,能更清晰地显示肿瘤的精确位置、大小、数量、形态及其与周围重要脑组织(如功能区、血管)的关系。增强扫描(注射造影剂)能显著提高微小转移灶、脑膜转移灶的检出率,对于制定治疗方案至关重要。对于本案例,增强MRI可以明确显示单发或多发的强化病灶,并评估其周围水肿带的严重程度。
计算机断层扫描(CT):在急诊情况下,当患者无法立即进行MRI检查或需要快速排除急性颅内出血、脑疝等危及生命的状况时,头颅CT是重要的筛查工具。但其对小于5毫米的病灶,尤其是位于颅后窝的病灶,敏感性远低于MRI。
病理学与分子诊断:影像学提示脑转移后,明确病理性质是制定后续治疗方案的基石。对于手术可及的单发或寡转移灶,神经外科医生可能会建议进行立体定向活检或手术切除,获取肿瘤组织。病理检查不仅能确认转移性癌,且通过免疫组化染色(如ER、PR、HER2、Ki-67)可与原发乳腺癌进行比对,确认来源。对获取的肿瘤组织进行基因检测,寻找可能的驱动基因突变(如PIK3CA、ESR1等),能为后续的靶向治疗提供关键依据。
其他辅助检查:正电子发射计算机断层显像(PET-CT) 有助于在全身范围内寻找其他潜在的转移灶。对于疑似软脑膜转移的患者,脑脊液检查进行细胞学分析可能具有诊断价值。血液或脑脊液中的肿瘤标志物(如CA15-3)动态监测,可作为评估治疗反应和监测复发的辅助手段。
综合上述检查,神经外科医生可以全面评估患者的病情:是单发、寡发(通常指1-3个)还是多发脑转移;病灶位于功能区还是非功能区;是否存在严重的脑水肿和颅内高压;患者的全身状况和原发癌控制情况如何。这些信息是决定采取手术、放疗、药物治疗还是多种手段联合的基础。
三、 综合治疗:神经外科主导的多学科协作
乳腺癌脑转移的治疗是一个系统工程,需要神经外科、肿瘤内科、放疗科、病理科、影像科等多学科团队共同决策。治疗目标是在控制颅内病灶、缓解神经症状、保护神经功能的前提下,尽可能延长生存期并提高生活质量。
1. 对症支持治疗与急诊处理:对于像本案例这样以急性颅内高压症状就诊的患者,紧急降颅压治疗是首要步骤。常用药物包括甘露醇、甘油果糖、高渗盐水等脱水剂,以及糖皮质激素(如地塞米松)减轻肿瘤周围水肿。同时需控制癫痫发作,预防电解质紊乱等并发症。
2. 局部治疗:
手术切除:适用于一般状况良好、颅外病灶控制稳定、且脑转移瘤为单发或少数几个(寡转移)、位于手术可及的非功能区、引起明显占位效应或诊断不明确的患者。手术能迅速解除压迫、降低颅内压、获取组织标本明确诊断和分子分型,为后续治疗创造条件。
放射治疗:是脑转移最主要的局部治疗手段。
全脑放疗:曾是多发脑转移的标准治疗,能有效控制全脑范围的微小病灶,但可能对认知功能造成长期影响。
立体定向放射外科:如伽玛刀、射波刀,通过将高剂量射线精准聚焦于肿瘤,对周围正常脑组织损伤小。特别适用于治疗直径较小(通常<3cm)的寡转移灶,或作为术后残腔的补充治疗。目前,对于有限数目的脑转移灶,立体定向放射外科的应用越来越广泛。
3. 全身性药物治疗:
化疗:传统化疗药物由于血脑屏障的存在,在脑转移治疗中疗效有限。但一些脂溶性较高或分子量较小的药物(如替莫唑胺、卡培他滨等)有一定应用。
靶向治疗:对于HER2阳性乳腺癌,新一代大分子单抗(如曲妥珠单抗-deruxtecan)以及能更好穿透血脑屏障的小分子酪氨酸激酶抑制剂(如拉帕替尼、图卡替尼等)在控制脑转移方面显示出显著疗效。
免疫治疗:对于三阴性乳腺癌等特定亚型,免疫检查点抑制剂(如PD-1/PD-L1抑制剂)联合治疗也在探索中,为部分患者带来了新的希望。
内分泌治疗:对于激素受体阳性的乳腺癌脑转移,在局部治疗基础上联合有效的内分泌治疗,有助于控制全身病情。
治疗方案的选择需高度个体化,综合考虑脑转移瘤的数量、大小、位置、症状、原发肿瘤的分子分型、全身疾病负荷以及患者的体能状态和治疗意愿。
四、 预后与长期管理
乳腺癌脑转移的预后虽仍严峻,但已非绝境。随着诊疗技术进步,患者的生存期和生活质量已得到显著改善。预后与多种因素相关:脑转移灶的数量和大小、是否伴有其他远处转移、患者的体能状态、原发肿瘤的分子亚型及对全身治疗的反应等。
长期管理至关重要:
定期随访监测:治疗后需定期(如每2-3个月)进行头颅MRI复查,评估疗效和监测新发病灶。
康复与支持治疗:针对神经功能缺损(如偏瘫、失语)进行规范的康复训练。积极处理疼痛、恶心、疲劳等症状,提供营养支持和心理疏导,对维持患者生活质量意义重大。
患者与家属教育:告知患者及家属可能出现的症状变化,如头痛加剧、新发抽搐、肢体无力、性格改变等,一旦出现需立即就医。
结论
乳腺癌术后五年突发头痛、呕吐,是一个强烈的临床警示信号,高度提示脑转移的可能。从病理生理上理解,这是颅内压增高的典型表现。神经外科的及时介入,依托头颅MRI等精准影像技术,是明确诊断的关键。治疗上,应以神经外科为核心,联合肿瘤多学科团队,根据病灶特点和肿瘤生物学行为,制定个体化的手术、放疗和药物治疗方案。本案例提醒所有临床医生和乳腺癌幸存者,即使度过术后数年平稳期,对神经系统症状保持警惕、进行必要的筛查,是实现早期诊断、有效干预、从而改善生存结局的重要一环。未来,随着更多能穿透血脑屏障的靶向药物和免疫疗法的研发,乳腺癌脑转移的治疗前景将更加广阔。
