排异之刃:移植后免疫博弈的双重奏——论白血病患儿移植后排异反应的辩证观
引言:并非简单的“好”与“坏”
在儿童白血病的治疗战场上,异基因造血干细胞移植(俗称移植)常被视为一种可能带来治愈希望的重要武器。移植成功远非终点,紧随其后的排异反应(医学上称为移植物抗宿主病,GVHD)往往成为患儿与家庭必须面对的下一个严峻挑战。对于许多患儿家长而言,“排异”一词常与痛苦、风险乃至失败联系在一起,令人闻之色变。在血液科医生的专业视角下,排异反应并非全然是“坏事”,其背后隐藏着复杂而精妙的免疫学博弈。^ 这种反应实质上是一把“双刃剑”:一方面,失控的免疫攻击会对患儿的皮肤、肝脏、肠道等重要器官造成损伤,甚至危及生命;适度的、可控的免疫反应,恰恰是移植的(供者细胞)在患儿体内成功植活并发挥“移植物抗白血病”(GVL)效应的关键体现,有助于清除体内残存的白血病细胞,降低远期复发风险。^ 本文将深入剖析白血病患儿移植后排异反应的本质、类型、临床意义及管理策略,旨在提供一个全面而辩证的认知框架。
第一部分:排异反应的本质与类型——宿主与移植物的攻防战
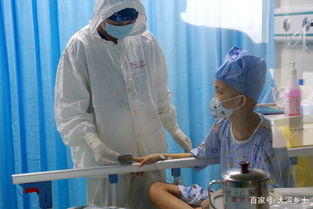
排异反应的核心,是免疫系统对“自我”与“非我”的识别与攻击。在移植的语境下,主要存在两种方向的免疫冲突。
1. 移植物抗宿主病(GVHD):主要的排异形式
这是异基因移植后最常见且被广泛讨论的排异类型。其本质是移植进入患儿体内的、来自供者的免疫细胞(主要是T淋巴细胞),将患儿的身体组织器官识别为“异己”并发动攻击。^ 根据发生时间和临床特点,GVHD可分为急性和慢性。
急性移植物抗宿主病(aGVHD):通常发生在移植后100天之内。^ 它起病较急,主要靶器官是皮肤、肝脏和消化道。^ 患儿可能出现从斑丘疹到全身性红皮病甚至水疱的皮肤病变;肝脏受损表现为黄疸、肝酶升高;肠道受累则导致痉挛性腹痛、水样腹泻甚至血便。^ 重度急性GVHD是导致移植相关死亡的重要原因之一。^
慢性移植物抗宿主病(cGVHD):通常发生在移植100天之后,可能由急性GVHD延续或转化而来,也可能独立发生。^ 其病理过程更类似一种自身免疫性疾病,影响更为广泛,可累及皮肤(出现硬化、苔藓样变)、口腔(干燥、溃疡)、眼睛(干眼症)、肺部(支气管炎闭塞)、肝脏以及关节等。^ 慢性GVHD病程迁延,严重影响患儿长期生活质量,但其发生有时也与较强的GVL效应相关联。^
2. 宿主抗移植物反应(排斥反应)
这种反应方向相反,是患儿自身残存的免疫系统对移植进来的供者造血干细胞进行排斥,可能导致移植物被清除,移植失败。^ 随着现代移植前预处理方案(使用高强度化疗/放疗)的完善,这种情况已较少见,但一旦发生,则意味着治疗挫折。^
第二部分:排异反应的“坏”与“好”——一把危险与希望并存的双刃剑
为何血液科医生会持有“排异反应不全是坏事”这一看似矛盾的辩证观点?这需要从排异反应的临床后果两面性来理解。
“坏”的一面:免疫攻击带来的直接损伤与风险
排异反应,尤其是中重度反应,其危害是直接且明确的:
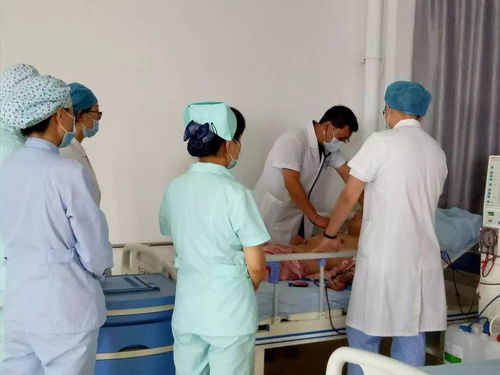
器官功能损伤:免疫细胞无差别攻击靶器官,导致皮肤破溃、肝功能衰竭、肠道黏膜脱落、肺部纤维化等,严重破坏患儿的生理功能。^
感染风险激增:为控制排异,必须使用强效的免疫抑制剂(如糖皮质激素、钙调神经磷酸酶抑制剂等),这进一步削弱了患儿本就脆弱的免疫防御能力,使其极易发生细菌、病毒、真菌的机会性感染,而感染本身也是移植后死亡的主要原因。^
生活质量下降:慢性GVHD引起的皮肤硬化、口腔干燥、眼部病变等,会给患儿的日常生活、学习和心理带来长期困扰。^
死亡风险:不可控的重度急性GVHD或多器官衰竭的慢性GVHD,可直接危及生命。^ 临床治疗的首要目标是预防重度排异的发生,并在其出现时积极干预。
“好”的一面:移植物抗白血病(GVL)效应的伴随礼物
这是排异反应辩证观中最核心的“利好”维度。供者免疫细胞在攻击患儿正常组织的也会识别并清除患儿体内残存的白血病细胞,这种效应被称为移植物抗白血病(GVL)效应。^ 某种意义上,GVHD是GVL效应一种“过火”或“脱靶”的表现。
降低复发率的天然屏障:大量临床观察表明,发生过轻度至中度慢性GVHD的患儿,其白血病复发率往往低于那些完全没有排异迹象的患儿。^ 这说明,持续存在的、可控的免疫活性,如同一支常驻的“清扫部队”,持续监视并消灭可能复发的恶性细胞。
治疗策略的利用:基于这一原理,临床上对于移植后复发高风险的患者,医生有时甚至会采取“诱导排异”的策略,例如谨慎地快速减停免疫抑制剂、或进行供者淋巴细胞输注(DLI),旨在激发GVL效应来对抗复发。^ 这种操作如同走钢丝,必须在严密监控下进行,力求在激发GVL和控制GVHD之间找到精妙的平衡。
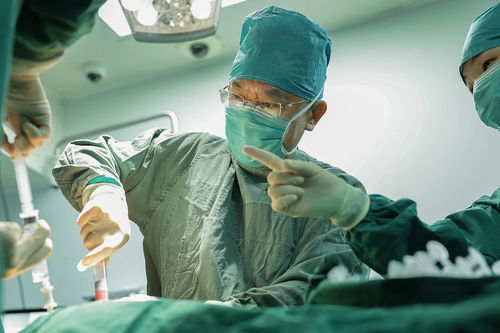
不同白血病类型的差异:GVL效应的强度因白血病类型而异。例如,在慢性髓系白血病(CML)和部分急性髓系白血病(AML)中,GVL效应较为显著;而在某些急性淋巴细胞白血病(ALL)中则相对较弱。^ 这解释了为何医生对不同患儿的排异现象会有不同的关注重点和期望阈值。
第三部分:走向平衡——排异反应的监测、防控与治疗艺术
面对排异这把双刃剑,现代移植医学的目标并非彻底消除排异(这可能导致复发风险增高或移植物被排斥),而是追求一种理想的“平衡状态”:即最大限度地保留有益的GVL效应,同时将GVHD的损伤控制在最低、最可管理的程度。^ 实现这一目标,是一项贯穿移植始终的系统工程。
1. 移植前与移植初期的预防基石
精细的供者选择:尽可能选择人类白细胞抗原(HLA)高分辨配型全相合或尽可能相合的供者(同胞全相合为首选),是降低严重GVHD发生率的根本。^
预防性免疫抑制方案:移植后立即常规使用免疫抑制剂,如他克莫司、环孢素、吗替麦考酚酯等,是预防急性GVHD的标准措施。^ 用药方案和剂量需个体化调整,并密切监测血药浓度。
2. 移植后的密切监测与早期识别
定期随访和敏锐观察至关重要。医生会要求患儿家庭密切关注:
皮肤:有无新出现的皮疹、红斑、瘙痒或硬化。^
消化道:大便次数、性状(是否变稀、水样)、有无腹痛、恶心呕吐。^
眼部与口腔:是否干燥、有砂砾感、疼痛或溃疡。^
肝脏:有无皮肤、巩膜黄染。
全身状况:有无不明原因发热、体重下降、活动耐力减退等。^
定期复查血常规、肝肾功能、免疫指标及必要的器官功能评估(如肺功能),是发现隐匿性排异的重要手段。^
3. 排异发生后的分层与综合治疗
一旦确诊GVHD,治疗立即启动,并根据其类型、严重程度和累及器官进行分层管理:
一线治疗:对于急性GVHD,糖皮质激素(如甲泼尼龙)是基础及首选药物。^ 它能快速强力地抑制过度的免疫炎症反应。
二线及挽救治疗:若激素治疗效果不佳或出现激素依赖,则需升级或转换方案。常用药物包括:
钙调神经磷酸酶抑制剂:如他克莫司、环孢素,常与激素联用或作为维持治疗。^
靶向药物:如JAK抑制剂芦可替尼,对激素难治性急性或慢性GVHD显示出良好疗效。^
其他免疫抑制剂:如吗替麦考酚酯、西罗莫司等。^
细胞治疗:间充质干细胞输注对部分难治性GVHD,特别是慢性GVHD有一定调节作用。^
局部与支持治疗:对于局限性皮肤GVHD,外用激素或钙调磷酸酶抑制剂药膏、窄谱中波紫外线光疗是有效手段。^ 强有力的支持治疗不可或缺,包括抗感染、营养支持、保肝、止泻、疼痛管理等,以帮助患儿度过难关。^
4. 长期生活管理与心态调整
战胜排异是一场持久战。患儿家庭需要:
严格遵医嘱:不可自行调整免疫抑制剂用量,这是维持平衡的生命线。
筑牢感染防线:注意个人卫生,佩戴口罩,避免去人群密集处,确保饮食清洁,按时接种必要的灭活疫苗。^
保障营养:在消化功能允许下,提供高蛋白、高热量、易消化的食物,必要时寻求临床营养师指导。^
关注心理健康:长期的病痛和治疗压力对患儿及家长都是巨大考验,寻求心理支持同样重要。
定期随访:即使情况稳定,也需终身坚持定期复查,以便及时发现并处理晚期并发症或慢性GVHD的进展。^
结论:在风险与希望之间寻求最优解
对于白血病患儿移植后的排异反应,我们应摒弃非黑即白的简单判断。它既是治疗过程中需要严阵以待的“敌人”,因其可能带来严重的器官损伤和生命危险;在某种程度上,它也是帮助我们巩固疗效、降低复发的“盟友”,因其承载着宝贵的移植物抗白血病效应。^
血液科医生所说的“排异反应不全是坏事”,其深意在于强调一种动态的、权衡的医疗哲学。现代移植医学的终极艺术,不在于消灭所有排异,而在于通过精准的供者选择、个体化的免疫抑制方案、严密的监测以及多学科的综合管理,引导患儿的免疫系统走向一种“有控制的共存”状态。在这种状态下,供者的免疫细胞能够聪明地识别并攻击残留的白血病细胞,同时最大限度地“容忍”患儿的正常组织,从而在治愈疾病与保障长期生活质量之间,为每一位勇敢的小战士找到那条最安全、最有效的康复之路。^ 这条路固然充满挑战,但对排异反应科学、辩证的理解,无疑是照亮前路、赋予患儿家庭信心与力量的一盏明灯。
