从细微便形到生命警报:解读结直肠癌的“大便变细带血”与环周肿物
引言:不容忽视的肠道信号
在消化系统疾病的诸多征兆中,排便习惯与粪便性状的改变往往是最直接、最应被警惕的早期信号。特别是当大便持续变细如铅笔,并混杂着或明或暗的血液时,这绝非偶然的肠胃不适,而可能是结直肠发出的“求救信号”。结直肠癌作为全球范围内高发的恶性肿瘤,其早期症状隐匿,但“大便变细带血”这一组合征象,常是肿瘤进展到一定阶段后向外界传递的关键信息。深入理解这一症状背后的病理生理、掌握其与肠镜下“环周肿物”这一关键发现的关联,并系统了解后续的诊疗路径,对于提升公众健康意识、促进早诊早治具有至关重要的意义。
第一部分:症状的病理生理学基础——为何会“大便变细带血”?
“大便变细带血”并非独立的症状,而是结直肠癌肿瘤生长特性在排泄物上的直接反映。其发生机制紧密关联,共同描绘出肿瘤在肠腔内的侵袭图景。
1. 大便变细:肠腔狭窄的物理征象

粪便在结肠内形成,其性状与直径主要取决于肠腔的容量、内容物的性质以及肠道的蠕动功能。当结直肠内壁生长出肿瘤,尤其是呈环周性或半环周性生长的肿瘤时,会逐渐侵占肠腔空间,形成物理性狭窄。正常成形的粪便通过这段狭窄的“隧道”时,会被挤压变形,从而呈现出持续的、进行性加重的细条状、扁带状或铅笔样外观。左半结肠和直肠的肠腔相对较窄,粪便在此处已基本成形,因此此部位的肿瘤更易导致显著的便形改变,并可能伴随排便费力、不尽感甚至肠梗阻的前期症状。
2. 大便带血:肿瘤组织脆性与侵蚀的必然结果
便血是结直肠癌最常见的症状之一,其表现形式多样,病理机制复杂:
肿瘤表面血管破裂:恶性肿瘤生长迅速,需要丰富的血液供应,其表面的新生血管结构异常、脆弱。当相对坚硬的粪便摩擦经过肿瘤表面,极易导致这些脆弱的血管破裂出血。血液直接混入粪便,若出血部位靠近(如直肠癌),常表现为便后滴血或粪便表面附着鲜红色血液;若出血部位较高,血液在肠道内停留时间较长,则呈暗红色或与粪便充分混合。
肿瘤坏死与溃疡形成:随着肿瘤体积增大,其中心部位可能因血供不足而发生缺血、坏死、脱落,形成溃疡。坏死的肿瘤组织和溃烂的黏膜会持续渗血,这种出血常与坏死组织、黏液混合,使粪便呈暗红色并带有特殊的腥臭味。
继发性炎症与浸润:肿瘤的存在会引发局部肠黏膜的慢性炎症反应,导致黏膜充血、水肿、糜烂,从而增加出血倾向。当肿瘤进展至晚期,侵犯肠壁深层血管甚至周围组织的大血管时,可能导致突发性的大量出血,危及生命。
“大便变细”与“带血”常常相继或同时出现,因为引起肠腔狭窄的肿瘤,其表面也正处于不断生长、破溃、出血的状态。这一组合症状高度提示肠道内存在占位性病变,尤其是恶性肿瘤。
第二部分:肠镜下的关键发现——环周肿物的临床意义
当患者因“大便变细带血”就诊并接受结肠镜检查时,肠镜下的直观发现是确诊和评估病情的关键。其中,“环周肿物”是一个具有重要预后意义的描述。
1. 什么是环周肿物?
环周肿物是指在肠镜下观察到的,沿肠壁呈环形或近乎环形生长的肿瘤性病变。它意味着肿瘤的生长已不仅限于肠壁的一侧或局部,而是环绕肠腔蔓延,导致肠腔周径的大部分甚至全部被肿瘤组织占据。这通常是肿瘤纵向生长一段时间后,横向浸润扩展的结果。
2. 环周肿物与肿瘤分期的关联
肠镜下肿物的形态是判断肿瘤分期的重要依据。根据内镜下特征:
早期癌:通常表现为息肉样隆起或平坦型病变,范围局限,基底清晰,肠腔无狭窄。
进展期癌(中晚期):环周肿物是典型表现。肿瘤常呈菜花样、溃疡型或隆起型,基底宽大,质地坚硬,表面覆有污秽苔及坏死组织,触碰易出血。肠腔因肿物侵占而出现明显狭窄,肠镜通过时阻力增大,严重时甚至无法通过。从病理浸润深度看,形成环周肿物的肿瘤通常已穿透肠壁黏膜下层,浸润至肌层甚至浆膜层(T3期或更晚)。这种生长方式极易导致肠梗阻,也是预后相对较差的一个指标。
3. 环周肿物的分型与特点
根据大体形态,环周生长的肿瘤可分为:
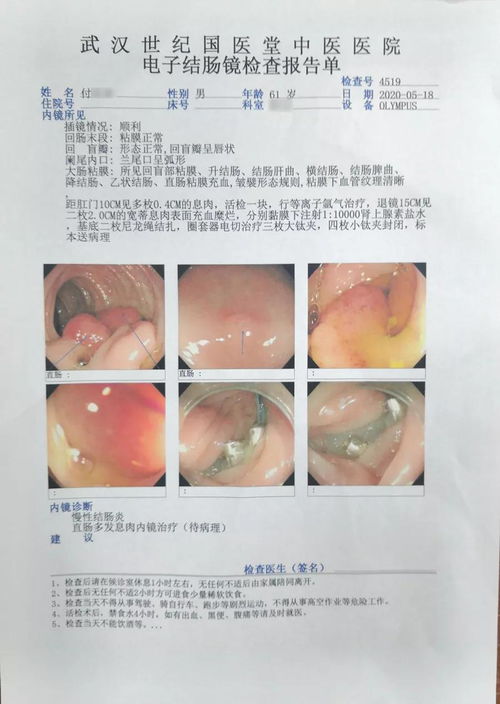
溃疡浸润型:中心为巨大溃疡,边缘呈堤坝状隆起并环周浸润。
肿块型:向肠腔内突出生长的巨大菜花状肿块,环周生长导致肠腔狭窄。
弥漫浸润型(硬癌):较少见但更具侵袭性,肿瘤沿肠壁各层弥漫性浸润,伴大量纤维组织增生,使肠壁均匀增厚、僵硬,肠腔呈管状狭窄,内镜下黏膜表面可能相对完整但色泽苍白、僵硬,活检时质地极硬。此型早期即可引起肠梗阻。
第三部分:从症状到确诊——综合诊断评估体系
面对“大便变细带血”的症状和肠镜发现的“环周肿物”,一套系统、精准的诊断评估流程随即启动,旨在明确肿瘤的性质、精确分期,并指导治疗。
1. 内镜精查与活检:肠镜检查是首要且不可替代的手段。除了直观观察,医生会进行染色内镜、放大内镜或窄带成像(NBI)检查,以更清晰显示病变的细微结构和血管模式。最关键的一步是钳取肿物组织进行病理活检,这是确诊结直肠癌的金标准。对于环周肿物,需多点、深部取材,以提高诊断准确性。
2. 影像学精准分期:
盆腔/腹部CT平扫+增强:是评估结肠癌及远处转移(尤其是肝、肺)的首选方法。能显示肿瘤的肠壁浸润厚度、周围脂肪间隙是否清晰、有无区域淋巴结肿大及远处器官转移。
盆腔MRI平扫+增强:对于直肠癌,盆腔MRI是局部分期的“金标准”。它能极其清晰地显示直肠壁的各层结构,精确判断肿瘤浸润深度(T分期),特别是评估肿瘤与直肠系膜筋膜(MRF)的距离。若肿瘤或转移淋巴结距离MRF ≤ 1mm,则定义为环周切缘(CRM)阳性或MRF受累,这是预测局部复发风险和指导新辅助治疗的关键指标。
直肠腔内超声(ERUS):可作为直肠癌局部浸润深度评估的备选或补充手段,尤其适用于早期病变。
3. 肿瘤标志物检测:如癌胚抗原(CEA)、糖类抗原19-9(CA19-9)等,虽不具特异性,但对辅助诊断、监测疗效和预警复发有重要价值。治疗前CEA水平显著升高(如>200ng/ml)是预后不良因素之一。
第四部分:综合治疗策略——针对环周肿物伴高级癌变
诊断为“结肠环周肿物伴高级别癌变”通常意味着肿瘤已属局部进展期。治疗目标是根治性切除肿瘤、预防复发和转移,其策略强调多学科团队(MDT)讨论下的个体化综合治疗。
1. 手术治疗:根治的核心
手术切除是可能获得治愈的最主要手段。根据肿瘤部位、分期及患者全身状况,手术方式包括:
根治性切除术:对于结肠癌,常行病变肠段切除加区域淋巴结清扫(如右半结肠切除、左半结肠切除等)。对于直肠癌,则根据肿瘤距肛缘的距离,选择低位前切除术(LAR)或腹会阴联合切除术(APR),在保证根治的前提下尽可能保留功能。对于环周肿物,术中确保获得阴性切缘(特别是环周切缘CRM阴性)至关重要。
2. 围手术期治疗:提升疗效的关键
新辅助治疗(术前治疗):对于局部进展期直肠癌(如cT3-4和/或淋巴结阳性,尤其是MRI评估CRM阳性或肿瘤浸润系膜深度>5mm者),标准方案是进行新辅助放化疗。术前放疗(如45-50Gy)联合以氟尿嘧啶或卡培他滨为基础的同步化疗,可以显著缩小肿瘤体积、降低分期、提高R0切除率(即显微镜下切缘无残留),并降低局部复发率。对于部分具有高危因素(如转移灶>3个、最大径≥5cm等)的可切除结肠癌肝转移,也可能推荐围手术期化疗。
辅助治疗(术后治疗):对于II期高危或III期结肠癌,以及所有接受根治性手术的直肠癌(无论是否接受新辅助治疗),术后通常需要接受辅助化疗,以消灭可能存在的微小转移灶,降低复发风险。常用方案包括FOLFOX或CapeOX等,疗程通常为6个月。
3. 转移灶的针对性处理:
若已发生肝、肺等远处转移,治疗决策更为复杂。对于可切除的转移灶,争取手术切除;对于不可切除但局限的转移灶,可考虑局部消融治疗(如射频消融、微波消融),特别是对于直径<3cm的病灶。全身化疗(±靶向治疗)是晚期或转移性结直肠癌的基石治疗。
4. 支持治疗与随访:
包括营养支持、疼痛管理、心理疏导等,贯穿治疗始终。治疗后必须进行规律随访,包括定期体检、CEA监测、肠镜和影像学检查,以便早期发现复发或转移,及时干预。
结论:警醒、筛查与科学应对
“大便变细带血”是结直肠癌向人体发出的一个清晰而严肃的警报。它背后所代表的,很可能是一个正在环周生长的肠道肿瘤。从察觉这一症状,到通过肠镜确诊“环周肿物”,再到接受以手术为核心的综合治疗,是一条完整的现代结直肠癌诊疗链条。这一链条的成功运转,依赖于公众对异常症状的足够警醒和及时就医,依赖于消化内科、内镜中心、影像科、病理科、肿瘤外科、肿瘤内科和放疗科等多学科的高效协作。对于高危人群(如有家族史、炎症性肠病、不良饮食习惯者),即便无症状,定期结肠镜筛查也是预防和早期发现结直肠癌的最有效手段。面对疾病,科学认知、规范诊疗、积极心态,是战胜结直肠癌的有力武器。
